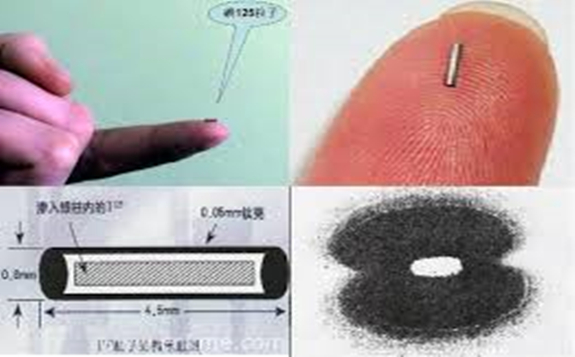
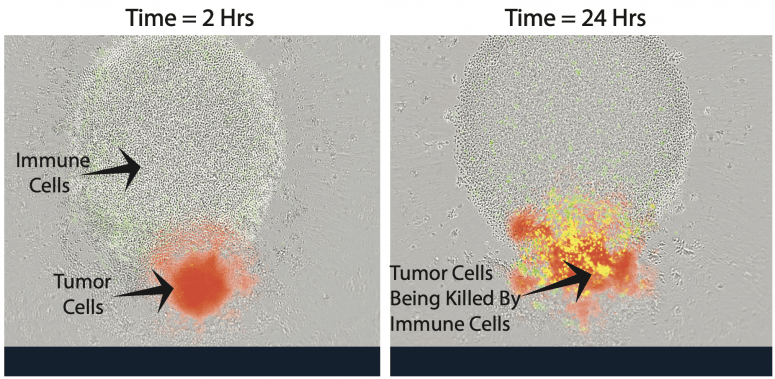
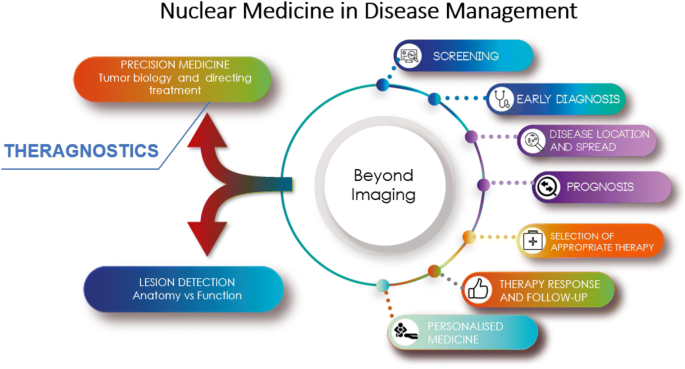
新的放射性药物S值数据库在治疗转移性骨癌时特别有用,在该转移性骨癌中,原发肿瘤(A)中的细胞侵入周围组织(B)并进入继发部位(C,D)
美国研究人员说,考虑到肿瘤的成分和质量,可以使放射性药物癌症治疗的剂量计算更加准确。佛罗里达大学和放射性药物成像与剂量测定法的Edmond Olguin及其同事对不同的放射性核素如何在形状,大小和组织矿化程度不同的肿瘤中沉积能量进行了建模。他们发现,针对骨骼中的小肿瘤计算出的剂量对此类特性特别敏感。研究人员说,他们的研究结果将提高放射性药物治疗的有效性,并准备立即被临床医生采用。
尽管大多数形式的放射疗法均以精确剂量的放射线靶向单个肿瘤,但放射药物疗法可通过向患者整体施用放射性核素标记的药物来治疗广泛分布的癌症。通过选择正确的放射性核素或将其与某种药物结合,临床医生可以使放射性药物选择性地蓄积在肿瘤中。这将最大化癌组织的剂量,同时将患者其他部位的辐射负荷保持在有害水平以下。
计算接收剂量的最准确方法是使用辐射传输模型和患者的个性化数字体模来模拟过程。但是,由于此技术需要大多数医院无法获得的专业知识和计算资源,因此最常用于研究环境。
取而代之的是,临床医生倾向于使用医学内部辐射剂量(MIRD)模式,这是一种将身体部位分类为辐射源(放射性药物在其中聚集)或辐射目标(在医学上有测量辐射的理由)的简单方法。在集中放射性药物的肿瘤中,这些区域是相同的。
当单个肿瘤既是目标又是目标时,计算输送剂量的关键是确定吸收分数-肿瘤内发射的能量比例,该能量在不逃避该区域的情况下沉积。这给出了每个放射性核素衰变的剂量,即“ S值”,其随所发射粒子的类型,其能量和肿瘤大小而变化。Olguin及其同事在《物理,医学与生物学》中写道,S值对肿瘤的元素组成也很敏感,到目前为止,该元素的组成通常被建模为软组织。
为了研究不同肿瘤成分的影响,研究人员使用超级计算机运行了蒙特卡洛N粒子传输(MCNP)模型。他们模拟了各种大小和轴向比率的球形和椭圆形肿瘤的光子,电子和α粒子辐照,其成分范围从100%软组织到100%矿物骨。
考虑到由软组织组成的球形肿瘤,研究小组发现,对于所有辐射类型和能量,其计算出的吸收分数与先前的估计值相差不超过几个百分点。但是,对于直径小于1.5厘米的矿化肿瘤,电子沉积的吸收部分比软组织肿瘤大25%。对于光子而言,其影响甚至更大,在所有肿瘤大小中,完全矿化的组织比未矿化的组织吸收的辐射要多71%。
Olguin及其同事还发现,在一定程度上椭圆形肿瘤可以近似为球形。尽管球形肿瘤的电子吸收分数与其椭圆形对应物的电子吸收分数相吻合在8%之内,但对于光子,这些误差特别大,对于椭圆率大于约0.98的肿瘤,这些误差超过20%。
由于剂量误差在小而矿化的肿瘤中最大,因此研究人员希望他们的研究在治疗患有骨癌骨肉瘤转移性扩散的患者中特别有用。为了帮助他们迅速将结果送入临床,他们编辑了一个查找表,该表显示了一系列肿瘤大小和组成的S值以及相关放射性核素的完整列表。
“由于S值仅是每个放射性核素衰变的辐射剂量,因此将其乘以衰变数就可以得出肿瘤剂量,”负责这项研究的佛罗里达大学的韦斯利·博尔奇解释说。“这个S值数据库可将肿瘤剂量的复杂性简化为两个数的乘积!”
该小组还计划将结果整合到社区开发的名为MIRDcalc的项目中,该项目将在一个软件包中计算核医学和X射线CT的器官剂量。