2月9日,国家药监局发布的信息显示,远大医药重磅产品钇[90Y]微球注射液获批,这标志着中国肝脏恶性肿瘤治疗领域迎来国际化精准介入治疗方案,填补了我国肝癌临床治疗的空白,具有里程碑式的意义。

近年来,医药行业风云变幻,但创新发展的底色却未动摇。在抗肿瘤领域,远大医药高瞻远瞩的加码放射性核素诊疗药物,并已在全球范围内实现了研、产、销等领域的全方位布局。在行业持续调整之下,远大医药凭借丰富的创新产品管线,犹如一匹黑马、牢牢占据优等生位置。钇[90Y]微球注射液的获批上市,也意味着历经三年多的持续深耕,远大医药在核药赛道的投入取得了关键性成绩。
01 肝癌治疗全球创新成果落地,钇[90Y]微球注射液带来新选择
中国是肝癌大国,每年肝癌新发病例达40万例,占全球肝癌新发病例近一半。肝癌有很强的隐匿性,多数患者发现时已是中晚期,仅20%~30%的肝癌患者可以手术切除,且5年内复发率仍高达60%~70%。
针对如此高发且易难及时发现的病状,创新治疗方式的引入是临床亟需。
钇[90Y]微球注射液可谓是肝癌的“克星”。其是一款针对肝脏恶性肿瘤的靶向内放射核素产品,采用全球领先的介入技术将钇[90Y]微球注射液注入肝脏肿瘤血管,释放高能量放射线杀灭肿瘤细胞。相比于其他治疗方式,钇[90Y]用于癌症治疗的优点非常明显:它在组织内平均射程2.5毫米,远低于用于常规放射治疗的射线,有效杀伤肿瘤细胞的同时避免对正常组织的损伤,且不需要对患者进行放射隔离。
2021年9月28日,中国首例特许准入钇[90Y]微球注射液临床治疗手术在海南乐城国际医疗旅游先行区的博鳌超级医院成功实施。
两个多月后,中国工程院院士、北京清华长庚医院院长董家鸿院士领衔的专家团队发布了手术后进展:术后三个多月增强CT及MRI影像检查复查结果显示,患者肿瘤病灶完全缓解,无活性病灶(mRECIST),AFP水平降至335.76ng/ml,这意味着患者肝部肿瘤已得到良好的控制。
值得一提的是,凭借优异的临床表现,钇[90Y]微球注射液是美国FDA正式批准的第一款针对肝脏恶性肿瘤的放射性微球产品,且截止目前仍是全球唯一一款用于结直肠癌肝转移选择性内放射治疗(SIRT)的产品。该产品已在全球超过50个国家和地区累计治疗超过12万人次,获得了美国、欧洲及中国的主流诊疗指南推荐,其安全性和有效性不言而喻。
2021年,钇[90Y]微球注射液获得英国国家健康照护专业组织推荐,对于Child-Pugh A级肝功能、不适合传统经动脉疗法的HCC成人患者,使用SIR-Spheres钇[90Y]微球注射液SIRT将给予全额资助和报销。
2022年1月8日,国家卫健委《原发性肝癌诊疗指南(2022年版)》正式发布。对于钇-90微球疗法,指南在2019年原版基础上,新增了桥接与降期治疗的用法推荐,表明国内专家对钇-90微球临床价值的进一步认可。
董家鸿院士表示,通过医生精准操作钇[90Y]微球注射液,实现对中晚期肝癌患者的降期治疗或潜在性根治,是我国肝癌治疗史上标志性的先进成果,具有里程碑意义。
目前,国内多家医院已经具备钇[90Y]微球注射液使用条件或正在积极准备,包括中国人民解放军总医院、北京大学肿瘤医院、复旦大学附属中山医院、复旦大学附属肿瘤医院、中山大学附属第一医院、中山大学附属肿瘤医院、华中科技大学同济医学院附属协和医院等。
值得一提的是,作为治疗方式的创新,钇[90Y]微球注射液拥有广阔的应用前景,其可以和靶向治疗、生物治疗、细胞治疗等开展联合应用。随着研究的深入,未来还可以产生很多新治疗方向。
02 10款创新产品齐驱,核药战略释放“原子”能量
“科技创新”是老牌药企远大医药近年来释放火力的聚焦点,也让企业走在了行业发展的前端。
远大医药持续创新转型,逐步完善了精准介入领域、肿瘤领域、抗病毒感染领域及呼吸科及五官科四大创新板块。目前,公司在抗肿瘤领域已储备16款全球创新产品,覆盖13个癌种,涉及肿瘤介入、RDC药物以及免疫治疗三个方向。
其中,放射性核素药物诊疗平台是公司在抗肿瘤领域重点打造的高端技术平台,远大医药联手重要的联营公司Sirtex和参股公司Telix以及ITM公司已储备了10款创新产品,涵盖6种核素。
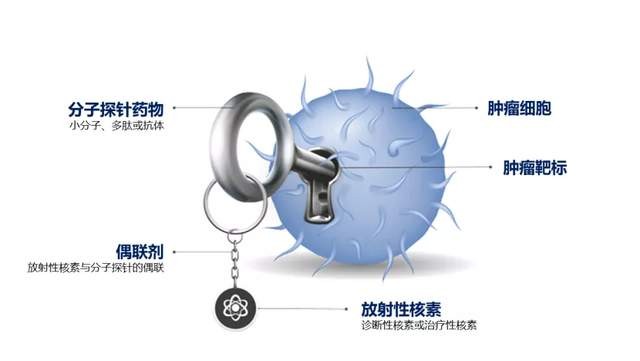
2021年12月27日,远大医药宣布与德国ITM Isotope Technologies Munich SE达成产品战略合作,引进后者用于诊断胃肠胰腺神经内分泌瘤的TOCscan,用于治疗胃肠胰腺神经内分泌瘤的ITM-11,以及用于治疗恶性肿瘤骨转移的ITM-41在内的3款全球创新型放射性核素偶联药物在大中华区的商业化权益。
在此之前,手握多个重磅核药品种的远大医药已经加速创新成果转化。2021年12月21日,远大医药重要战略合作伙伴Telix Pharmaceuticals Limited用于诊断前列腺癌的RDC药物TLX591-CDx在美国和澳大利亚获批上市,并在巴西获得特别授权,准许正式获批前销售。此外,用于诊断透明细胞肾细胞癌的TLX250-CDx已获FDA批准突破性疗法并于澳洲完成I期临床研究首例患者给药;用于治疗胶质母细胞瘤的TLX101已获FDA孤儿药资质认定。
本土+全球研发生产的双体系发展路径成为远大医药在创新赛道快速挺进的关键。此次钇[90Y]微球注射液在海南乐城“先行先试”以及最终获批上市,是公司创新布局摘得的重要果实。而TLX591-CDx等一系列在研药物的研发进展也将助力其在国内的落地推进。
据远大医药介绍,多款RDC药物在中国的注册工作均在积极推进中,其中TLX591-CDx预计将于2022年第一季度向国家药监局递交临床研究申请。
远大医药表示,未来公司将加大对放射性核素诊疗药物领域全球创新产品的投入及开发,丰富和完善产品管线及产业布局,不断提升公司在该领域的全球研发实力,为该产业的发展提供助力,打造国际领先的放射性核素药物诊疗平台,为全球患者提供更先进更多样的治疗方案。
03 政策春风不断,远大医药打造核药诊疗平台
产业的落地,离不开政策的支持。我国核药的研发、生产、使用机构受到《放射性药品管理办法》的严格管控。2021年以来,随着政策春风持续推动,核医学行业发展按下了快进键。
2022年1月,为进一步加强放射性药品生产管理,保证放射性药品质量安全有效,国家药监局发布《关于进一步加强放射性药品管理有关事宜的通告》。根据《通告》,含有短半衰期放射性核素的药品,可以边检验边出厂。
2021年6月24日,国家原子能机构联合科技部、国家卫生健康委、国家医疗保障局、国家药品监督管理局等八部门正式发布《医用同位素中长期发展规划(2021—2035年)》(以下简称《规划》),这是我国首个针对核技术在医疗卫生应用领域发布的纲领性文件,对提升医用同位素相关产业能力水平、保障健康中国战略实施具有重要意义。
中华医学会核医学分会主任委员李思进表示,《规划》充分肯定了核医学在重大疾病早期诊断、微小病灶的精准清除以及合理诊疗方面具有独特的作用,作为全球创新型放射性同位素药物,钇[90Y]微球注射液必将启动并加速我国核医学的长远发展和深刻变革。
平安证券发布的研报认为,此次《规划》的出台,是扩大核医学普及性、产业链自主可控、加快创新核药及设备研发的重要信号,有望根本性改变监管部门对核医学细分领域重视不足的问题,过去影响行业发展速度和制约创新的因素有望得到解决,政策春风推动下,核医学行业将迎来更快速的发展。
先于政策的落地,凭借敏锐地嗅觉,除了钇[90Y]微球注射液等创新核素药物的布局外,远大医药还与江苏原子医学研究所、生态环境部核与辐射安全中心等机构达成合作,实现了研发、生产、销售、监管资质等多领域的全方位布局,公司在核医学赛道的综合竞争力进一步提升。
科技创新是企业发展的原动力。持续全球化创新布局、手握丰富的创新产品管线,远大医药通过与重要联营公司 Sirtex Medical和参股公司 Telix以及ITM等公司及机构的合作,公司在核药抗肿瘤等多个细分领域龙头地位逐渐显现,正朝着国际领先的放射性核素药物诊疗平台持续迈进。
钇[90Y]获批上市可谓是远大医药持续投入创新发展过程中的重要里程碑,也是公司迈向新目标的起点。核药治疗领域是一高门槛、高壁垒的赛道,参与者较少。随着钇[90Y]的获批上市,国内核药双寡头的局面已经被打破,中国核药治疗领域将会开启时代新篇章。伴随着中国核药市场空间的打开,远大医药未来可期!