尽职调查:在不同场景中逐步验证 DirectSPR,例如在拟人化头部模型中,是将软件成功转化为临床工作流程的基本步骤。即使在 DirectSPR 算法开发的形成阶段,OncoRay 的 Christian Richter(右)与研究员 Patrick Wohlfahrt 在这里展示,也专注于转化结果。(提供:HZDR/Rainer Weisflog)
合作带来创新:这无疑是一项雄心勃勃的、多中心的德国研发计划的口头禅,该计划利用学术研究人员、临床医生和行业的跨学科专业知识,在放射肿瘤学诊所提供颠覆性的进步——提高准确性、安全性和质子治疗系统在此过程中的组织保留能力。有问题的突破源于用于质子治疗计划的双能 CT (DECT) 的临床部署和所谓的DirectSPR 软件的应用1,2用于更准确地预测患者体内的质子范围。统一愿景的所有部分——认为转化研究满足临床应用——重新构想质子治疗的规划、交付和管理,以满足个体癌症患者的独特需求。
DirectSPR 的临床推广由位于德累斯顿的OncoRay 的Christian Richter 领导的转化团队率先推出。OncoRay 研究人员与海德堡德国癌症研究中心(DKFZ)的同事密切合作进行算法开发和验证——这两个研究所共同组成了国家肿瘤放射研究中心 (NCRO)——而工业支持来自癌症治疗业务线在西门子Healthineers。
OncoRay本身是一个政府资助的研究中心,专注于辐射的新技术和治疗方法翻译成肿瘤的临床应用,汇集了三个创始机构的优势:卡尔·古斯塔夫·卡鲁斯大学医院德累斯顿,德累斯顿工业大学和亥姆霍兹Dresden-罗森多夫。“虽然 OncoRay 的主要驱动力是提高治疗效果和患者结果,”Richter 解释说,“我们还寻求与领先的医疗技术制造商的合作伙伴关系,以确保我们的研发能够覆盖更广泛的放射肿瘤学界——基于 DECT 的 DirectSPR 在两方面。”
创新开箱
如果这是背景故事,那么在质子治疗计划中支持这种新范式的具体细节是什么?特别是,更准确地预测不同组织类型中的质子范围和停止行为的基础是什么?成功的关键是 DECT 技术的创新应用及其光谱成像能力,用于预测治疗计划的质子范围。与传统 CT 不同,这种成像方式涉及获取两个单独的 X 射线能谱——这种方法反过来又允许表征在不同能量下表现出不同衰减特性的组织(但至关重要的是,无需将患者暴露于更高-射线剂量)。
与此同时,DirectSPR 是一种用于 DECT 图像后处理的算法——特别是确定不同组织类型中质子的个体停止行为。同时,DirectSPR 通过使用复杂的降噪和根据扫描的身体感兴趣区域定制应用程序,最大限度地提高了停止信息的定量质量。通过这种方式,DirectSPR 使医学物理学家能够更好地解决给定患者群体以及同一患者中组织成分的差异,并在治疗计划中考虑这些差异。(为完整起见,SPR 是停止能力比,表示质子的能量损失与穿过患者的距离相对于水中能量损失的关系。)
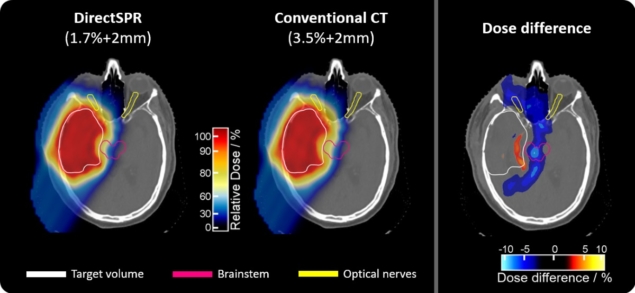
查看差异:与用于治疗计划的传统 CT(左)相比,DirectSPR 提高的准确性导致目标体积周围健康组织的剂量显着减少(右,剂量差异图中的蓝色区域)。同时,还可以实现更好的肿瘤覆盖(红色区域)。(提供:OncoRay、尼尔斯·彼得斯、克里斯蒂安·哈恩)
2019 年春季,Richter 和他在 OncoRay 的同事成为第一个部署基于 DECT 的 DirectSPR 作为质子治疗常规临床工作流程的一部分的团队——这是改进德累斯顿大学质子治疗静态肿瘤部位治疗计划的关键一步。卡尔·古斯塔夫·卡鲁斯大学医院的一部分)。从那时起,对于 300 多名患者,基于 DECT 的 DirectSPR 使德累斯顿诊所——在持续和可重复的基础上——将前列腺癌靶区周围受照射的健康组织的体积(安全界限)减少了大约 35%和脑肿瘤治疗。
当然,临床影响是根据多个坐标定义的,尤其是 SPR 计算和相关质子范围预测的准确性——这两者都决定了肿瘤周围的安全范围,进而决定了组织保留的程度。由于基于 DECT 的 DirectSPR 的临床引入,OncoRay 实现了质子范围计算的不确定性(现在 <2%)与传统的基于 CT 的规划方法(其中不确定性已设置为总质子的 3.5%过去 30 年的范围)。结果:骨盆治疗的质子射程平均减少 3.6 毫米,头部治疗平均减少 2.6 毫米。“对于个体脑肿瘤治疗,”Richter 说,“因此,我们能够将脑干等关键结构的剂量减少 16%,视交叉和视神经的剂量减少 7%,大脑的平均剂量总体减少 4%,如代表性患者病例所示。这是将患者治疗后副作用风险降至最低的相关进展。”
翻译在行动
DirectSPR 转化为临床产品的时间表可以追溯到 2015 年初,当时来自 OncoRay 和 DKFZ 的科学家开始致力于 DirectSPR 方法的开发和优化。他们的目标是:最大限度地减少与患者组织中质子范围预测相关的不确定性,从而提高质子治疗的靶向精度和剂量分布精度。这个由 NCRO 资助的为期四年的项目 - 与 Siemens Healthineers 密切合作 - 始于 2015 年在德累斯顿大学质子治疗中心引入 DECT 用于临床质子治疗计划 - 这是世界上第一个可以回顾性评估DirectSPR 方法用于不断增长的治疗性 DECT 患者扫描数据库(而不仅仅是使用体模或计算机模拟)。
“即使在 DirectSPR 算法开发的形成阶段,OncoRay 和 DKFZ 也专注于转化结果,”Richter 说。早期对复杂算法的定义——尤其是随后在不同场景(包括拟人模型和生物组织)中全面逐步验证的重点——是成功翻译的基础。“这让我们、社区和负责任的临床医生相信该方法的优越性,”Richter 补充道。“Siemens Healthineers 于 2016 年加入,早期的对话围绕我们共同的临床和研究目标建立了信任和理解。”
正是在这一点上,合作进入了临床前产品开发阶段,OncoRay、DKFZ 和 Siemens Healthineers 共同致力于 DirectSPR 算法的优化和校准。随着 DirectSPR 软件于 2019 年春季的商业发布,Siemens Healthineers 现在确保 DirectSPR 在其整个 DECT 扫描仪产品组合中的兼容性,并为每个 CT 模型进行专门校准。
临床路线图
就下一步而言,OncoRay 的 Richter 和同事——以及他们在 Siemens Healthineers 的行业同行——都专注于加速质子治疗社区对 DirectSPR 的临床接受(参见“质子观点:DirectSPR 机会”)。就 OncoRay 而言,它与许多欧洲质子治疗中心保持双边合作,并且在欧洲粒子治疗网络(欧洲放射治疗和肿瘤学会的一个小组)中也很活跃(ESTRO)。“正在准备一份共识文件,为质子治疗诊所中 DirectSPR 的临床实施定义最佳实践指南和标准化,”Richter 解释说。他希望该文件将在即将举行的 ESTRO放射肿瘤学 CT 创新临床转化研讨会的讨论中提出。
与此同时,OncoRay 和 DKFZ 团队已经与 Siemens Healthineers 合作探索新的转化途径,包括使用基于 DECT 的 DirectSPR 对移动目标(例如肺和腹部的肿瘤部位)进行质子治疗规划。“我们在 OncoRay 和 DKFZ 的任务是支持进一步改进用于放射治疗环境中的下一代 CT 扫描仪的 DirectSPR,”Richter 总结道。
Proton 观点:基于 DECT 的 DirectSPR 机会
越来越多的临床兴趣将 DirectSPR 部署为质子治疗工作流程的核心组件。在这里,Physics World与一些早期采用质子设施的医学物理学家交谈,以评估进展、下一步和预期的临床优势。
赵天宇,密苏里州圣路易斯华盛顿大学医学院
我们正在招募患者参加美国国立卫生研究院 (NIH) 赞助的研究,使用 DECT 扫描仪收集数据,以提高对肿瘤部位和周围器官组织成分准确性的估计。目标:减少质子治疗中实际递送剂量与计划剂量之间的差异。我们计划通过使用临床协议扫描的体模来量化 DirectSPR 对质量密度和质子 SPR 预测的准确性。此特定于站点的准确性信息将用于调整使用 DECT 扫描的质子患者的稳健性优化中的不确定性设置。最终,希望我们的工作将减少质子的范围不确定性,并在质子治疗中实现更好的规划质量和更少的剂量预测错误。
Ming Yang ,德克萨斯州休斯顿MD 安德森癌症中心
我们目前正在将我们的机构 syngo.via 服务器(来自 Siemens Healthineers)升级到 VB40——这是实施 DirectSPR 的先决条件。完成后,我们将在 DirectSPR 可用时立即开始调试过程。最初的优先事项是测试 DirectSPR 与我们现有治疗计划系统的兼容性,并评估与软件对质子停止能力的估计相关的不确定性。就我个人而言,我相信 DirectSPR 将以多种方式使我们的患者群体受益。一个直接的影响将是减少接受接近处方剂量的高剂量的正常组织——从而减少正常组织的毒性。较小范围的不确定性参数也将更容易实现满足计划目标的稳健治疗计划。最后,
Benjamin Ackermann,海德堡离子束治疗中心(HIT) 和 Friderike Longarino,海德堡大学医院
HIT 使用免费测试许可证完成了 DirectSPR 的临床验证——对于有兴趣了解更多信息的诊所来说,这是一个方便且风险低的选择。验证过程包括完整的放射治疗工作流程和拟人模型的剂量学测试,由多种不同的组织等效材料组成。我们现在正在安装购买的软件许可证,并期待使用 DirectSPR 执行第一次患者扫描,从表现出很少或没有分次内运动的头部和骨盆等身体区域开始。通过 DECT 扫描和 DirectSPR 图像处理,与 SECT 相比,我们希望在离子束治疗中实现更好的 SPR 预测,进而实现更好的范围预测。
美国马里兰州质子治疗中心Sina Mossahebi
在我们最初的 DirectSPR 研究中,我们的目标是量化常规 SECT 和 DECT在体内和患者计划之间的剂量计算差异,目的是减少强度调制质子治疗 (IMPT) 计划中的范围不确定性。SECT 和 DECT 扫描均来自同一患者,用于评估在每个图像集上生成的治疗计划之间的剂量学差异。该研究的主要目标是量化和比较风险器官 (OAR) 的靶覆盖范围和剂量,以及为接受 IMPT 的患者获得的 SECT 和 DECT 扫描之间的计划稳健性。此外,我们将使用患者特定的 QA 验证 SECT 和 DECT 剂量计算,同时探索 DECT 在目标描绘和植入方面的实际优势。
Gabriel Fonseca 和 Frank Verhaegen,荷兰Maastro 诊所
我们对 DirectSPR 的评估正在多个方面进行。通过广泛的体模测试,我们研究了 TPS 用于剂量计算的 SPR 信息,比较了通过基于 DECT 的 DirectSPR 和 SECT 方法获得的 SPR 预测。前者更准确,其差异不到 SECT 所得结果的一半。另一个重点是校准程序,这可能需要一系列体模尺寸来匹配患者体型的变化——即诊所的额外工作。虽然 DirectSPR 可以提供更准确的 SPR 值,但治疗计划的不确定性取决于几个因素。因此,Maastro 团队正在评估改进的 SPR 地图对 50 多名患者队列的稳健优化计划的影响。总之:虽然我们预计 DirectSPR 能够将质子范围精度从 1 毫米提高到几毫米(对于一些深部肿瘤),但很明显,在常规临床部署之前,需要彻底量化所有不确定性和风险来源。从长远来看,严格的质量保证程序将需要支持临床工作流程。
Ole Nørrevang,丹麦奥胡斯大学医院丹麦粒子治疗中心
我们正在采取分阶段的方法在奥胡斯推出基于 DECT 的 DirectSPR。我们首先实施虚拟单能图像并优化器官和目标勾画以及停止能力估计的使用。现在我们可以使用 DirectSPR 软件,我们的调查正在三个方面进行:验证 DirectSPR 产生的 SPR 值;研究减少范围不确定性对减少大脑中 OAR 剂量的影响;并了解与在脑肿瘤治疗计划中使用 SPR 图像相关的工作流程、患者安全和过渡问题。我们现在的重点是治疗脑肿瘤,因为我们可以排除 DECT 图像中运动伪影的影响。不过,随着时间的推移,我们将制定计划,将 DirectSPR 应用于其他治疗部位。
Koen Salvo ,比利时鲁汶粒子质子治疗中心
我们目前正在定义我们的 DECT 模拟协议,成人协议已经完成,并且正在与 Siemens Healthineers 就儿童协议进行对话。一旦这些协议最终确定,我们将激活我们的 DirectSPR 软件并使用动物体模上的质子射线照相术对其进行验证。使用 DirectSPR,我们希望更准确地计算质子范围。如果是这样,我们可以减少目标边缘,进而减少目标附近 OAR 的剂量——这是治疗脑干附近脊索瘤的重大进步。