近红外光操控的DNA纳米传感器用于特定细胞器中酶活性的精准成像分析
近日,中国科学院国家纳米科学中心研究员李乐乐课题组在亚细胞水平酶活性精准成像分析研究中取得进展。相关研究成果以Organelle-Specific Photoactivation of DNA Nanosensors for Precise Profiling of Subcellular Enzymatic Activity为题,发表在《德国应用化学》上。
真核细胞内复杂信号网络的调控依赖于每个蛋白质/酶的区室化分布。开发能够原位、高时空分辨的检测亚细胞器内酶活性的成像方法,对于理解其功能和转运机制十分重要。由于其高灵敏度、高选择性和实时成像等优点,基于小分子、蛋白质、纳米技术等设计的荧光传感器已被广泛用于生物分子的成像分析。然而,如何在亚细胞水平上时-空可控的成像酶活性仍是难题。这是因为传统传感器无法精准定位特定亚细胞区室,且在分子识别和信号响应上处于“始终开启”的模式,制约了成像的亚细胞分辨率和时空精准度。
李乐乐课题组致力于开发活细胞和活体内“时-空”可控的分子成像新方法,提出了利用上转换发光远程操控化学传感的新原理,以实现“时-空”可控的精准分子成像(J. Am. Chem. Soc. 2018, 140, 578),并将该方法拓展应用于“时-空”可控的RNA精准成像及信号放大(J. Am. Chem. Soc. 2019, 141, 7056;Angew. Chem. Int. Ed. 2019, 58, 14877)、时间分辨的pH动态成像(Nano. Lett. 2020, 20, 874)、DNA分子逻辑运算及多元成像(Anal. Chem. 2021, in press),以及分子识别调控及肿瘤精准诊疗(Nat. Commun. 2019, 10, 2839;Sci. Adv. 2020, 6, eaba9381)。
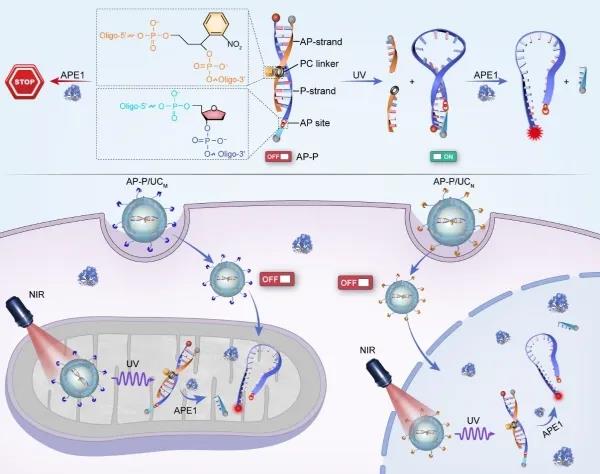
在前期工作的基础上,课题组发展了细胞器特异性光激活纳米传感器技术,选择性的在特定细胞器(如线粒体和细胞核)内对酶活性进行精准成像分析。该传感器平台是通过对基于DNA的传感分子工程化设计,并与上转换纳米颗粒以及细胞器定位信号相结合而构建的。传感器“按需”的可控定位和近红外光介导的原位激活有效地将成像功能限定到特定的细胞器,显著提高了亚细胞分辨率,并避免了非特异性信号干扰。通过程序化的亚细胞区室定位以及近红外光激活,实时监测到了酶分子在氧化应激下在不同细胞器间的动态转运行为。此外,由于近红外光具有良好层组织穿透深度,该传感器件可对活体内亚细胞水平酶活性进行特异性成像分析。该方法为亚细胞水平精准分子成像提供了新工具,有助于解析蛋白质/酶的区室化分布和机制。
国家纳米科学中心博士研究生邵玉蕾为论文第一作者,李乐乐为论文通讯作者。研究工作得到国家自然科学基金、中科院战略性先导科技专项(B类)等的支持。
