癌症标靶药物与免疫疗法都是癌症治疗主力军,已成功延长许多癌症病患的生命。然而科学家并不以此自满,还在持续开发不同类型的抗癌新药,“放射核种药物”(radiopharmaceutical)正是另一种值得期待的新颖药物。
传统放射线治疗的缺点
放射线用于治疗癌症已超过百年(注1),时至今日仍有约半数癌症病患在治疗某阶段会接受放射线治疗。虽已历经一世纪多,但放射线疗法进展仍相当缓慢──放射线必须由病患“体外”照射入“体内”肿瘤区域,破坏癌细胞的DNA借此消灭肿瘤。此做法下放射线也会通过正常组织,导致杀死癌细胞时许多正常健康细胞也遭波及,因此副作用不小,如掉发、丧失味觉、性功能障碍及腹泻等皆有可能发生。
放射核种药物的前身
一是1940年代治疗某些甲状腺癌病患、称为放射性碘(radioactive iodine)的疗法,此法利用碘在人体内会自然积聚于甲状腺的特性,当病患服用放射性碘后,就能聚积在甲状腺并杀死手术后残留的甲状腺癌细胞。
相隔70多年,2013年另一种治疗转移到骨骼的癌症药物“二氯化镭223”(radium 223 dichloride,Xofigo)获准用于治疗转移性“前列腺癌”,当癌细胞在骨骼内生长时,会损坏骨骼组织,此时身体会尝试修复这些损伤,由于放射性元素镭与钙原子十分近似,因此会当成钙而融入骨骼修复活动最旺盛的区域(如癌细胞正在增长的区域),此时放射性镭就能发挥作用,杀死周边癌细胞。
除了上述2种放射性药物,似乎没有其他药物能不假外力导向肿瘤所在器官组织,因此科学家必须花费更多心思,研发能针对不同癌症发动攻击的放射核种药物。
放射核种药物研发的突破进展
研究在2018年终于有了突破性进展,当年FDA批准诺华公司(Novartis)研发治疗消化道“神经内分泌肿瘤”(neuroendocrine tumors,NET)的放射核种新药Lutathera(lutetium Lu 177 dotatate)。
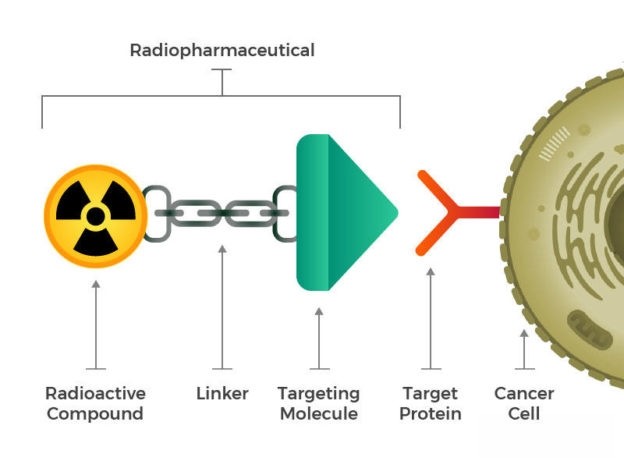
神经内分泌瘤的癌细胞表面经常会有高量“体抑素受体”(somatostatin receptor)蛋白,顾名思义,这些受体会与一种称为“体抑素”的生长素抑制因素蛋白结合,先前已有科学家研发出类似体抑素的蛋白药物以缓解病患症状、抑制肿瘤生长,现在科学家进一步将放射性元素镏177(Lu177,注2)借长度为8个氨基酸的胜肽,与体抑素类似蛋白接合在一起,成为放射核种新药Lutathera:体抑素类似蛋白将放射性元素携带至癌细胞表面,让放射性元素能就近发挥作用毒杀周边所有癌细胞。
放射核种药物研发的预期
有了上述重要里程碑,如今科学家更积极开发用于治疗肺癌、大肠癌及血癌等多种癌症的放射核种药物。只要癌细胞表面有异常高量的特定蛋白质、可区分癌细胞与正常细胞的分子标靶,且患处具适当血液循环能使药物经由血液输送抵达癌细胞表面,那么放射核种药物就有机会发挥毒杀癌细胞的作用,帮助治疗癌症。
结语
如今放射线治疗终于有了新转机,放射核种药物将能更精准针对癌细胞。过去几年,测试这类新药的研究和临床试验数量不断激增,试验结果显示放射核种药物能更彻底消灭癌细胞,且无论短期或长期副作用皆可降低。专家相信,再10~15年,这类药物必能将癌症治疗推向另一个境界。
注1:当放射性药物附着(或进入)癌细胞后,放射性物质衰变释放的能量会破坏邻近细胞DNA,当细胞DNA遭受无可挽回的损害时细胞就会死亡。此外,癌细胞对放射线造成的DNA损伤耐受力低于正常细胞,更容易死亡。注2:镏177发布的放射线粒子能量不会太强,只影响周围1毫米范围,所以对邻近正常组织的影响小。
(首图来源:NIH)