
近年来,肿瘤免疫疗法在肿瘤治疗中取得了重大突破,但其有效性在不同患者以及不同肿瘤类型之间存在很大的差异。因此,早期预测肿瘤患者对免疫治疗的响应情况,对于改善患者的治疗预后至关重要。颗粒酶B作为免疫应答中最主要的效应分子之一,存在于细胞毒性T淋巴细胞所释放的细胞颗粒中,可以进入肿瘤细胞介导细胞凋亡,是细胞杀伤的标志性分子,且其表达水平的改变,优先于肿瘤体积的变化,因此可以在免疫治疗早期通过对颗粒酶B的成像,实现长期疗效的预测。
研究团队基于前期研发的能够有效靶向颗粒酶 B 的小分子探针68Ga-grazytracer [1],开展了颗粒酶B靶向PET显像预测肿瘤免疫治疗疗效I/II临床试验。共招募了24例拟行免疫治疗的肿瘤患者进行临床转化研究,所有患者未见与药物相关的不良反应。该团队首先使用动态PET/CT评估了68Ga-grazytracer的体内代谢动力学。发现68Ga-grazytracer经肾脏从体内快速排出,肿瘤对其摄取随着时间的推移逐渐下降,但肿瘤-肝脏摄取比值呈上升趋势。7例患者手术标本颗粒酶B的免疫组织化学染色研究发现肿瘤组织中颗粒酶B的表达水平与68Ga-grazytracer的肿瘤摄取呈显著正相关。68Ga-grazytracer在"非沙漠"免疫表型肿瘤中的摄取显著高于免疫"沙漠"肿瘤,提示68Ga-grazytracer PET/CT在无创区分患者肿瘤免疫表型中的作用。
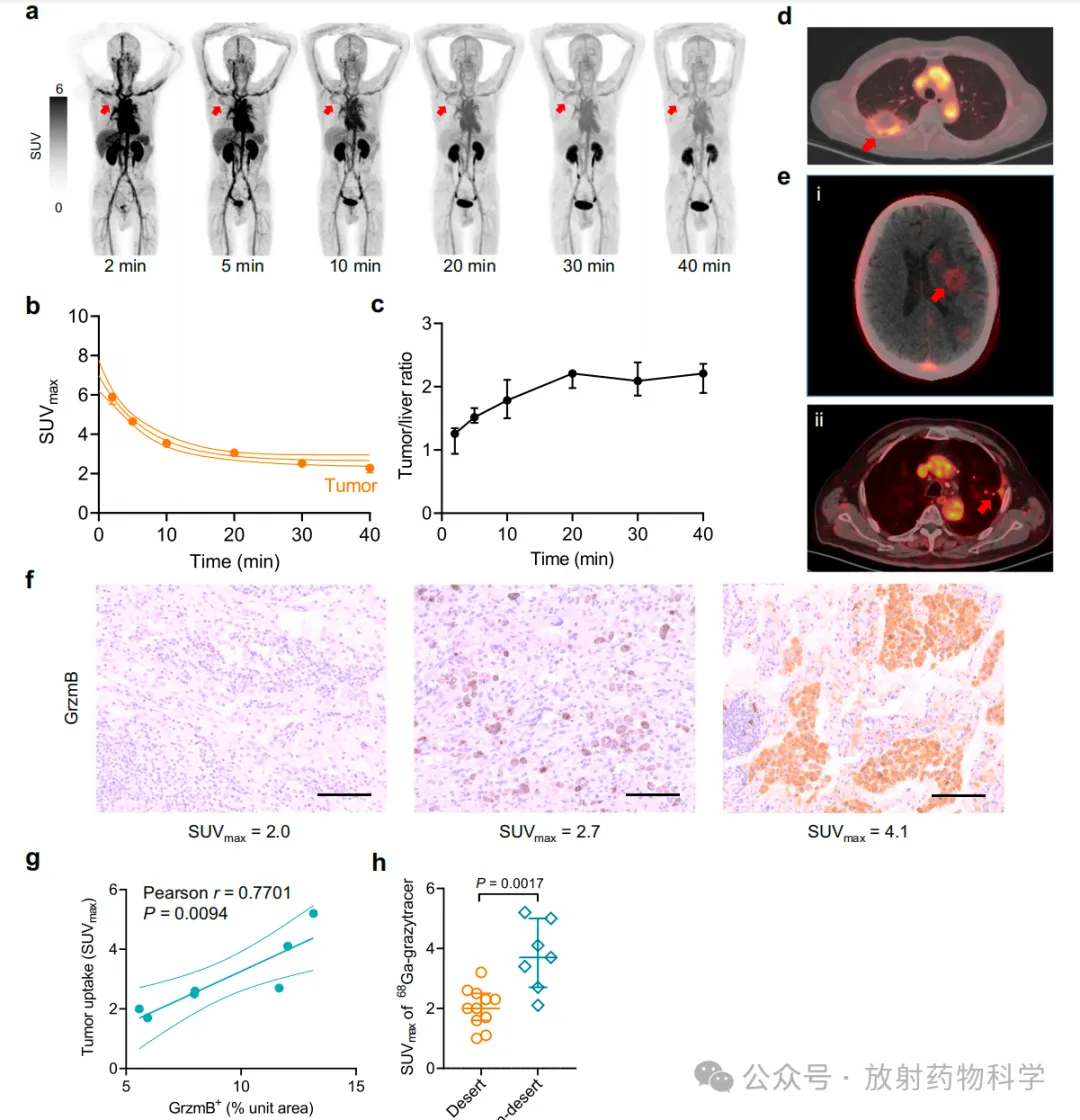
在对肿瘤免疫治疗反应预测方面,该团队发现在患者治疗6月后,应答组与未应答组间,仅68Ga-grazytracer SUVmax存在显著差异,且基于68Ga-grazytracerSUVmax的预测效能高于PD-L1免疫组织化学染色、治疗前后肿瘤长径变化值(ΔSLD)、治疗前后18F-FDG SUVmax变化值(ΔSUVmax)。在随访研究中,与RECIST 1.1/Lugano和PERCIST/Lugano标准相比,基于68Ga-grazytracer PET的预测标准(以SUVmax 2.3为界值)具有更好的长期疗效预测能力。
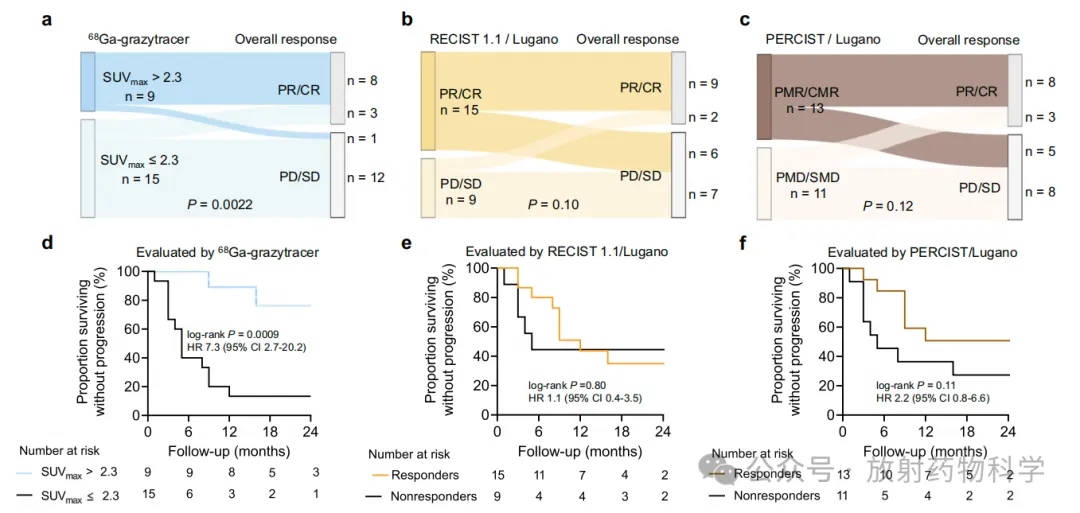
该研究的发表充分反映了核医学分子探针在肿瘤免疫治疗患者筛选、疗效评估及预后预测方面的应用潜力,为后续深入研究奠定了良好基础。
北京大学肿瘤医院李囡、杨志教授,北京大学基础医学院刘昭飞教授为该研究的通讯作者,2021级博士研究生沈秀铃和基础医学院2020级博士研究生周昊毅为该研究的共同第一作者。北京大学肿瘤医院临床流行病学研究中心李文庆教授,核医学科朱华研究员、肿瘤医院胸内一科、淋巴瘤科给予本研究大力帮助。该研究得到了国家重点研发计划、国家自然科学基金委国家杰出青年基金,北京市重点研发专题等项目的大力支持。