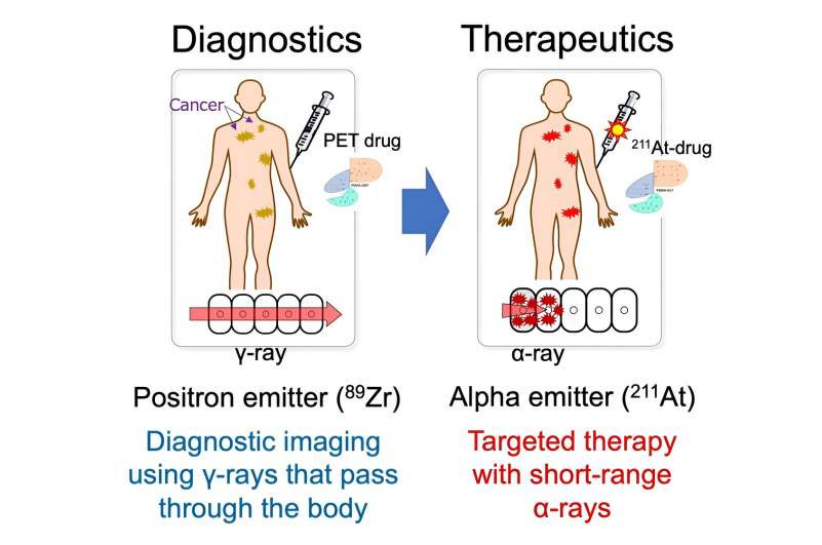
诊疗学概念:集诊断与治疗于一体的新型医疗技术。
图片来源:Tadashi Watabe博士(大阪大学)
胰腺导管腺癌(PDAC)是世界上最致命的癌症之一,5年生存率低于10%。许多PDAC肿瘤无法在早期阶段被发现,因为常规的成像方法包括fluorodeoxyglucose正电子发射断层扫描(PET))无法发现它们。为了更有效地对抗这种癌症,由大阪大学研究人员领导的一个团队正在将诊断和治疗程序结合成一个单一的综合过程,即诊疗学。
在最近发表在《Journal of Nuclear Medicine》上的一篇文章中,该团队开发了一种放射诊疗策略,使用一种新的放射性抗体来靶向glypican-1 (GPC1),一种在PDAC肿瘤中高度表达的蛋白质。诊疗学,特别是放射诊疗学,已经受到越来越多的关注,因为通过放射标记用于靶向癌细胞中某些分子的化合物,诊断和治疗可以依次进行。
该研究的主要作者Tadashi Watabe博士解释说:“我们决定以GPC1为靶点,因为它在PDAC中过度表达,但在正常组织中仅低水平存在。”
该团队使用了一种针对特定分子的单克隆抗体(mAb)来靶向GPC1。该单克隆抗体可用放射性锆(89Zr)或放射性砹(211At)来标记。他们研究了异种移植小鼠模型,将人胰腺癌细胞注射到小鼠体内,使这种肿瘤发展成可以通过实验治疗和监测的完整肿瘤。给这些小鼠静脉注射的为89Zr标记的GPC1 mAb。同时给予211At标记的GPC1单克隆抗体,以检测其抗肿瘤作用。
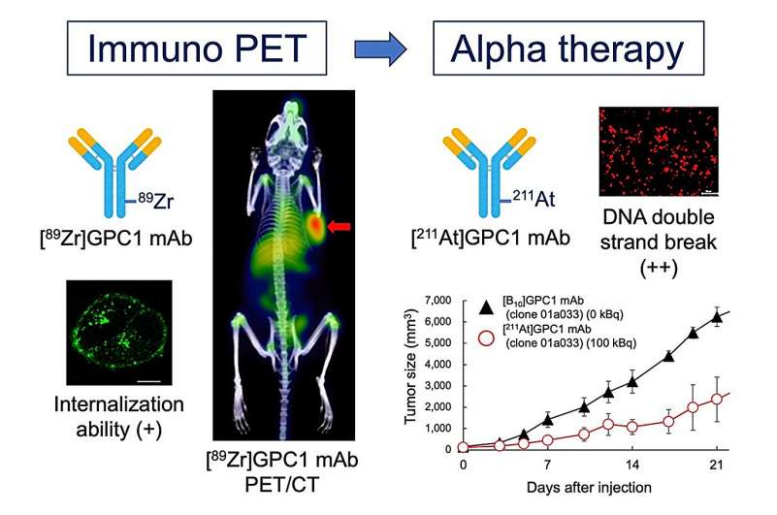
靶向glypican-1 (GPC1)的诊疗:
(左)使用胰腺癌模型小鼠(红色箭头表示肿瘤)进行Zr-89标记的GPC1抗体的PET成像;
(右)使用At -211标记的抗GPC1抗体对胰腺癌模型进行α放射治疗。
图片来源:Tadashi Watabe 博士(大阪大学)
本文第二作者Kazuya Kabayama解释道:“我们通过PET扫描监测了7天内89Zr-GPC1 mAb的内化情况。mAb在肿瘤中有很强的摄取,这表明这种方法可以支持肿瘤的可视化。我们证实,这是由其与GPC1的结合介导的,因为GPC1表达被敲除的异种移植模型显示出明显较低的摄取。
研究人员接下来使用211At-GPC1 mAb的α疗法对这一模型进行了测试,该方法可以支持基于放射性标记的治疗分子递送至靶点。211At-GPC1 mAb可诱导肿瘤细胞DNA双链断裂,并显著抑制肿瘤生长。对照实验表明,当mAb内化受阻时,这些抗肿瘤作用不会发生。此外,未放射性标记的GPC1 mAb没有诱导这些效应。
Tadashi Watabe博士说:“我们研究的两种放射性标记的GPC1 mAb在PDAC中都显示出可喜的结果。89Zr-GPC1 mAb显示出高肿瘤摄取,而211At-GPC1 mAb可用于靶向α治疗,以支持抑制PDAC肿瘤生长。"
这些极具影响力的数据证明了在PDAC中使用诊疗方法的潜力,这是一种迫切需要新的诊断和治疗方案的疾病。未来,有望通过PET成像实现PDAC的早期检测,并使用α疗法进行全身治疗。