由于现有的测试材料在质子治疗剂量测定中产生很大的不确定性,导致“射程”的相对差异高达8%。因此,这些现有材料不能为质子治疗剂量测定提供准确的质量保证。
相比之下,NPL开发的新材料在1%~2%的精度内模仿质子治疗中的人体组织特性,可更加有效地测量复杂质子治疗计划和临床试验中的剂量。这种新型组织模拟材料已被用来开发模拟头颈部肿瘤患者放射治疗的装置。这项研究已发表在Physics in Medicine Biology上。

这是第一个制定组织等效材料的模型,不仅考虑光子相互作用,还考虑质子阻止本领、核吸收和散射相互作用。研究还将优化材料的组织等效性与现有商业组织等效材料进行比较,以评估性能以及改进方面,见图1。
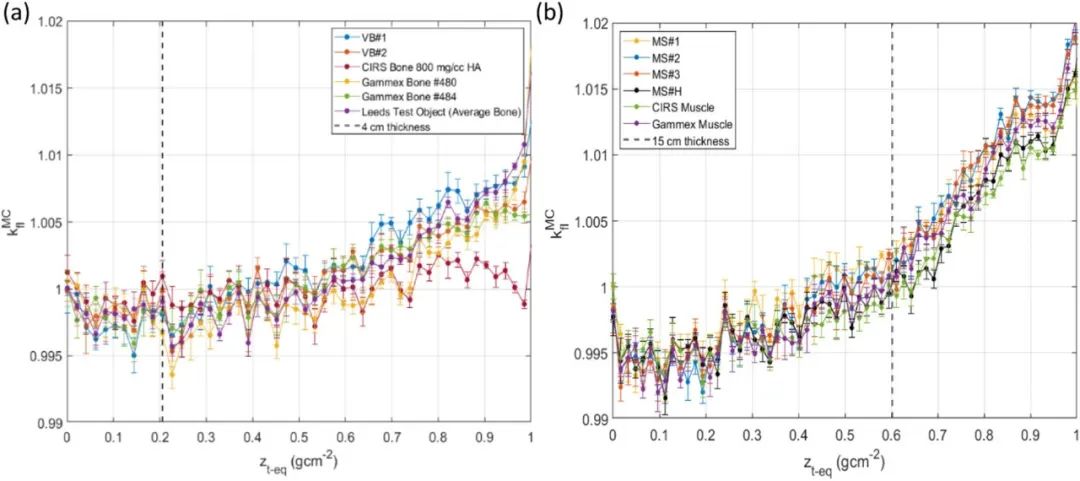
图1.新配方和商业材料的通量校正因子;(a)椎骨组织等效材料;(b)肌肉组织等效材料;参考虚线突出显示了质子可能穿过的患者体内每个靶区组织的最大组织厚度(骨骼为4厘米,肌肉为15厘米);每个误差条都呈现A类不确定性
这些材料使质子中心能够在临床使用前检查和测试质子治疗的具体治疗情况,使用内部探测器直接测量剂量,并将其与治疗计划软件的预测值进行比较。这些测试可提高质子中心进行质子治疗的准确度。
NPL科学家Ana Lourenço表示:“我们正在与医学物理与工程研究所(IPEM)合作,制定质子参考剂量测定的新实践规范(CoP)。即将推出的IPEM CoP将利用NPL的PSPC为质子治疗提供剂量校准服务。”
这一进展将减少剂量输送的不确定性,确保最佳的肿瘤控制,并提高质子治疗的准确性。CoP一致标准的建立不仅将使治疗机构内和治疗机构之间的患者获益,而且为质子治疗临床试验的发展奠定基础。
NPL科学领域负责人Russell Thomas表示:“我们团队多年来一直致力于测定质子束流的剂量,还开发了用于质子放射治疗的专用标准。在此基础上,我们能够进一步完善临床电离室反应的理解。此外,我们还制定了临床审查方案,确保患者得到最佳治疗,并且专门开发了自己的材料来模拟质子束流中组织、骨骼等的反应。”