美国食品和药物监督管理局(FDA)批准使用68Ga-Dotatate,一种用于正电子发射断层扫描(PET)成像的放射性诊断剂,以定位成人和儿童患者中的生长抑素受体阳性神经内分泌肿瘤。该商业产品是一种用于制备68Ga-Dotatate注射剂的单剂量试剂盒,由总部位于法国圣吉尼斯-普利的Advanced Accelerator Application公司生产,该商品已被命名为NETSPOT™.
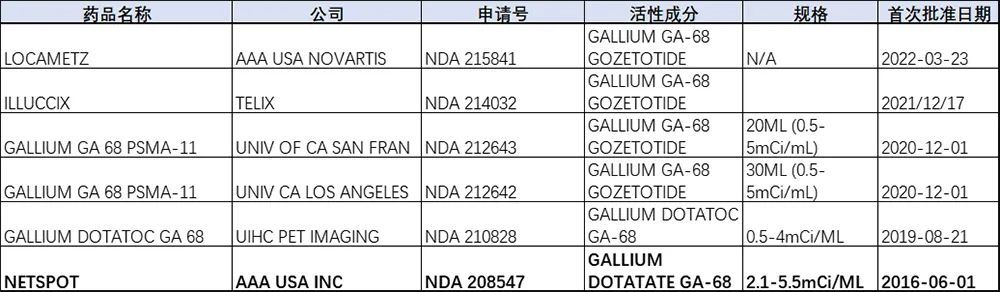
美国FDA批准Ga-68相关药品信息
神经内分泌肿瘤,每年在欧洲和美国约有47300人受其影响。肿瘤会在身体神经内分泌系统内产生激素的细胞中发育,位于胃、肠、胰腺和肺等器官中。
神经内分泌肿瘤具有生长抑素受体,生长抑素是一种调节内分泌系统的激素。68Ga-Dotatate是一种生长抑素的正电子发射类似物,通过与这些受体结合而起作用。68Ga-Dotatate的摄取反映了神经内分泌肿瘤中生长抑素受体密度的水平。
68Ga-Dotatate于2014年3月获得了FDA和欧洲药品管理局的孤儿药认定。“孤儿药”又称为罕见药,用于预防、治疗、诊断罕见病的药品。美国对孤儿药的定义为目标疾病患者少于20万;而在欧洲的定义为影响1万人中的不到5人。
Advanced Accelerator Applications公司宣布,NETSPOT将由俄亥俄州都柏林的Cardinal Health公司在美国代销,这家医疗服务公司运营着美国最大的放射性药物网络。该公司目前已批准使用Eckert&Ziegler的GalliaPharm®Ga 68发生器。
在其新闻稿中,FDA引用了三项确定NETSPOT安全性和有效性的研究,这些研究均由田纳西州纳什维尔范德比尔特大学医学中心的研究人员领导。第一项将神经内分泌肿瘤的68Ga-Dotatate图像与一种已批准药物的图像进行比较,然后通过CT或MRI进行确认。第二项目使用组织病理学方法评估68Ga-Dotatate图像。第三项研究证明了示踪剂用于神经内分泌肿瘤的诊断、分期和治疗管理的安全性和有效性。第三项研究的结果发表在2016年5月出版的《核医学杂志》上,也是发表在《应用放射学通讯》上的一篇文章的主题。