HNSCC是全球第七大最常见的癌症和癌症相关死亡原因,每年有878,000例新发病例和444,000例死亡病例。通常,HNSCC在局部晚期但可治愈的阶段被诊断出来,对于超过80%的病例,放疗联合或不联合放射增敏化疗是推荐的一线治疗。放疗时将更高剂量(通常70 Gray左右)递送至肿瘤,即总靶区体积(GTV),对于实现治愈是必要的。
然而,由于肿瘤与周围的关键危及器官(OAR)非常接近,因此HNSCC患者的放疗计划和实施非常复杂。在过去十年中,与光子技术相比,调强放疗(IMRT)的实施提高了放射剂量分布的一致性,具有更好的靶区覆盖率和更少的关键OAR剂量。然而,不能完全避免对周围OAR的照射,与HNSCC患者的急性和长期毒性相关。
质子通过布拉格峰在一定深度的组织中积累能量,由于能量积累发生在组织中的相对狭窄的深度范围内,与光子治疗相比,质子治疗能够向靶区体积递送高剂量,同时最大限度地减少对相邻OAR递送的剂量。比较质子治疗与IMRT的临床前和剂量学研究一致证明,质子治疗时OAR剂量显著减少,表明质子治疗可降低急性和长期毒性。鼻咽癌中所有OAR的剂量都会降低,如口咽癌、下咽癌和喉癌时,腮腺、喉和脊髓的受照剂量降低。同样,在比较鼻咽癌使用调强质子治疗(IMPT)和IMRT治疗计划之间的剂量测定时,IMPT计划时,29个OAR中有13个的平均剂量显著降低,包括口腔、大脑、脊髓和喉。
对现有质子治疗剂量学研究的主要批判是缺少考虑设置错误和解剖学变化。此外,尚不清楚当质子治疗和IMRT治疗计划的剂量水平都在规定的耐受范围时,OAR的剂量减少是否会产生显著的临床影响。由于观察到的差异可能被高估,有必要进行临床评估。HNSCC患者进行质子治疗的临床证据有限,缺乏质子治疗的Ⅰ级证据。如何确定患者是否从质子治疗中获益最高一直属于挑战。因此,在大多数国家,符合质子治疗报销的既定适应证仍然很少。尽管如此,全世界大约有100个拥有230多个治疗室的质子治疗中心在运作,并且正在报告质子治疗HNSCC的初步经验。
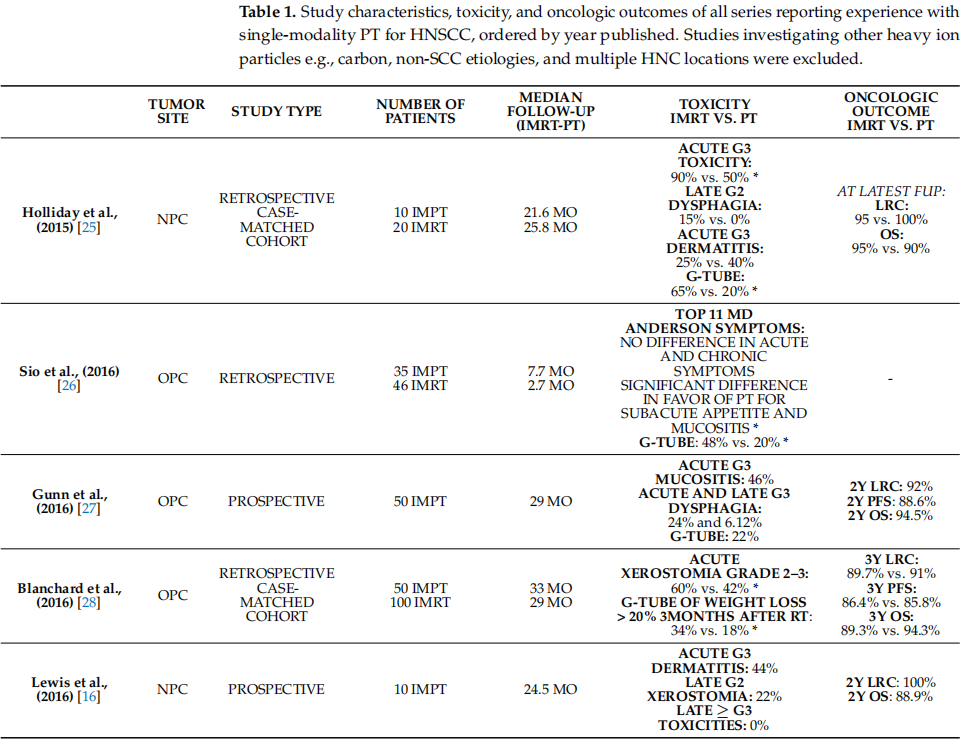
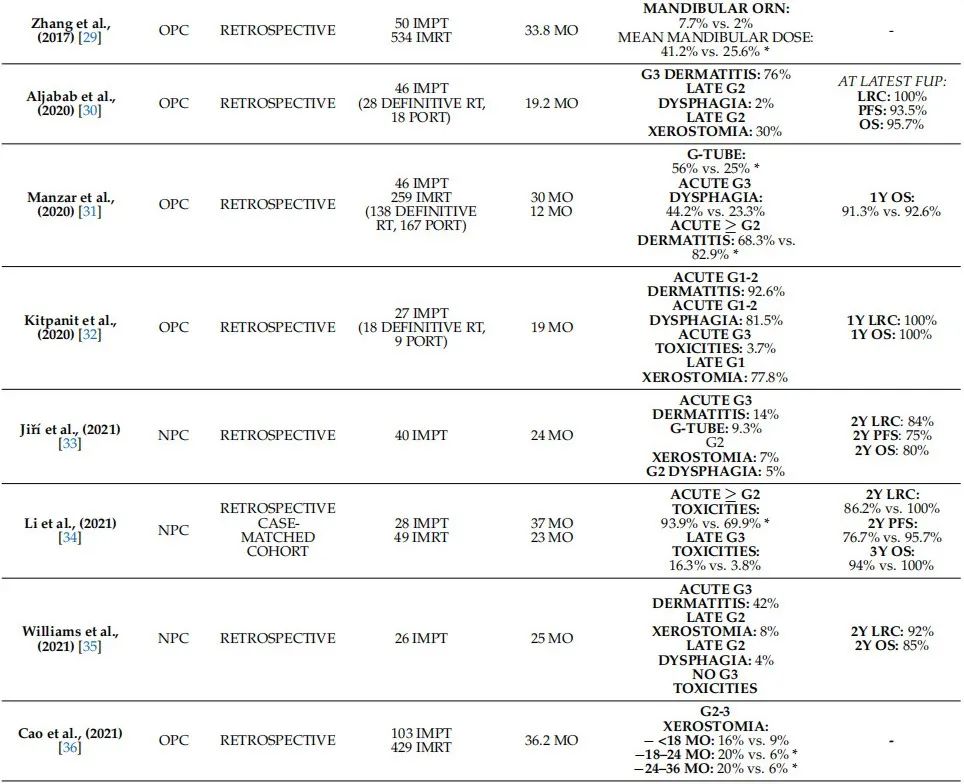
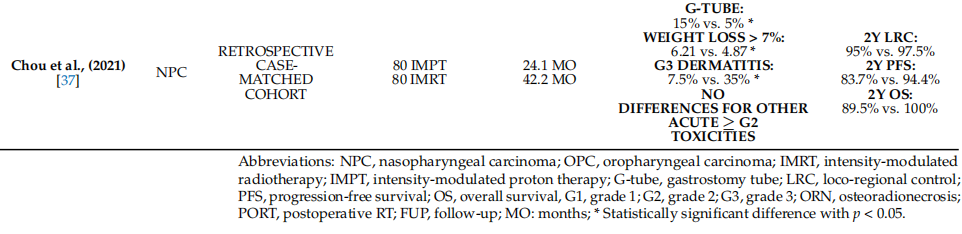
迄今为止,在确定的环境中HNSCC使用质子治疗的临床经验有限。大多数评估头颈癌(HNC)质子治疗的研究要么属于非鳞状细胞癌,要么属于再程照射。随着从事质子治疗机构数量的增加,正在报告更多积极的结果,尽管这些结果基于小型研究。表1提供了HNSCC单模态质子治疗后毒性和肿瘤学结果,不包括其他重离子、非SCC病因和多个HNC病灶位置的研究。