每个人的不同研究人员旨在通过结合与肿瘤和高危器官的独特放射敏感性相关的因素,为放射治疗计划提供更加个性化的方法。(礼貌:Shutterstock/Mark Kostich)
放射治疗的目标是向肿瘤目标提供规定的辐射剂量,同时限制对周围正常组织的损伤。目前,这是使用基于人群的治疗计划优化来实现的,该优化基于预先定义的基于剂量的目标和风险器官 (OAR) 限制,这些限制是从广泛的患者群体对辐射的聚合反应中发展而来的。不幸的是,这种标准化治疗计划的有效性和毒性各不相同,因为患者及其肿瘤具有个体生物学特征。
为了提供更加个性化的放射治疗计划方法,密歇根大学的研究人员开发了一种新的调强放射治疗 (IMRT) 优化策略,该策略直接将患者特定的剂量反应模型纳入计划过程。他们在医学物理学中描述的技术基于最大化整体治疗效用的预测值——定义为局部控制的概率减去毒性概率的加权和。
这种称为优先效用优化 (PUO) 的新规划方法通过结合与肿瘤和 OAR 的放射敏感性相关的个性化因素来增强标准方法。例如,OAR 的放射性毒性会受到年龄、吸烟状况、基因表达、分子标记和心脏病等既往疾病的影响。其他同时进行的治疗也可能影响放射治疗的效果。

研究人员:主要作者 Daniel Polan(左)和首席研究员 Martha Matuszak。(礼貌:D波兰)
为了验证他们的策略,首席研究员Martha Matuszak及其同事使用 PUO 方法为五名非小细胞肺癌 (NSCLC) 患者制定了 IMRT 计划。他们报告说,与用于治疗的传统计划相比,PUO 计划改善了所有患者的局部控制。
“非小细胞肺癌患者代表了一个高度异质的群体,疾病的范围和定位存在差异,”主要作者丹尼尔波兰解释说。“结合其他解剖变异性,这些因素会极大地影响治疗计划,包括不同优化方法的预期收益。因此,对于我们方法的初步可行性测试,我们选择了五个案例来代表患者大小、肿瘤大小、位置和侧向性的多样性,以及影响预测结果的剂量协变量的多样性。”
为了创建针对患者的 IMRT 计划,研究人员首先使用商业治疗计划系统来计算基于小束剂量对感兴趣区域贡献的影响矩阵的剂量。然后,他们解决了两个优化问题,以生成可以导入回 TPS 的最佳子束权重。
第一个优化问题通过基于个体化剂量反应模型优化疗效和毒性之间的权衡,使总体计划效用最大化,从而受到典型临床剂量限制。第二个最小化传统的基于剂量的目标,受到与第一个相同的剂量约束,同时保持从第一个优化确定的最佳效用。
对于所有五名患者,PUO 方法成功地生成了最佳的子束权重,在保持基于剂量的约束的同时最大化了效用。在这项研究中,研究人员将这些 PUO IMRT 计划与临床交付的 3D 适形放射治疗 (CRT) 计划以及回顾性生成的仅剂量优化 (DOO) IMRT 和体积调制弧治疗 (VMAT) 计划进行了比较。
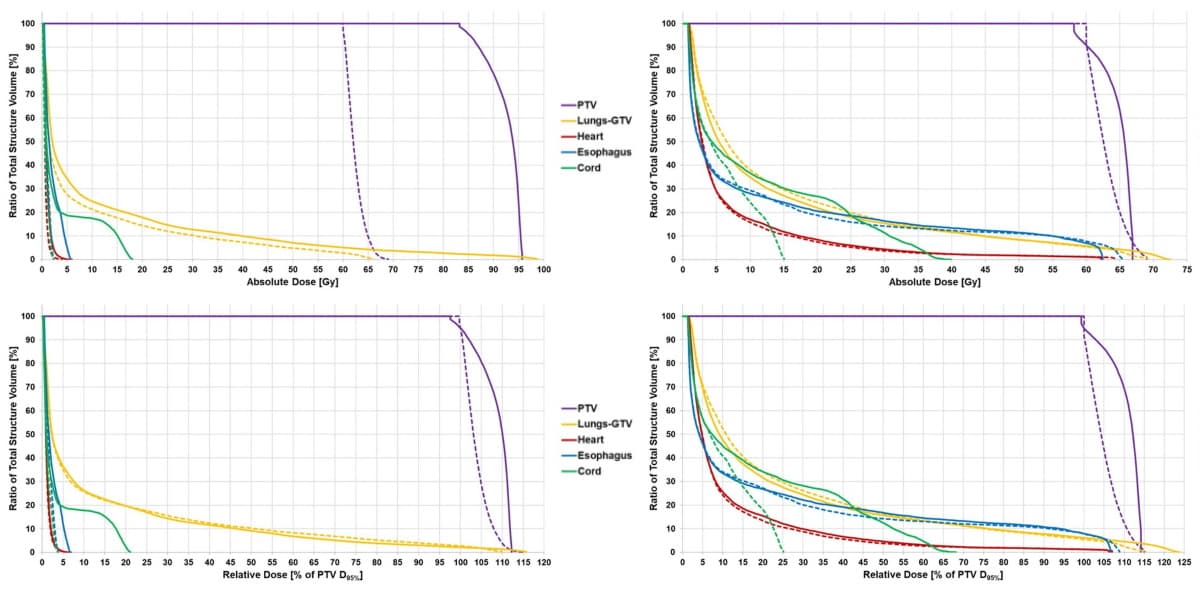
剂量学比较:两个肺癌患者的仅剂量优化(DOO,虚线)和优先效用优化(PUO,实线)计划的绝对和相对剂量体积直方图。对于一名患者(左图),PUO 导致计划目标体积 (PTV) 的剂量大幅增加,而食道和脐带剂量的增加较小。对于另一名患者(右图),PUO 略微提高了 PTV 覆盖率并降低了肺和食道剂量。(礼貌:Med. Phys. 10.1002/mp.15940)
与 3DCRT、VMAT 和 DOO IMRT 计划相比,PUO 方法分别平均提高了 40%、32% 和 31% 的计划效用。PUO 计划表明,局部控制平均提高了 17%,毒性与传统计划相似。
正如预期的那样,PUO IMRT 计划的获益程度因患者而异。Polan 报告说,对于一名患者,与传统 DOO 相比,PUO 的效用提高了 70%。“这相当于预测的无进展生存概率绝对提高了 32%,而辐射引起的肺毒性的预测概率仅增加了 2%,”他说。“这种实质性的权衡有可能大大提高疾病的生存能力,同时最大限度地减少对患者治疗后生活质量的影响。”
然而,对于另一位患有大肿瘤的患者来说,改善是微乎其微的。Polan 解释说,对于较大的肿瘤,由于整体剂量要求增加和避免与正常组织接壤的能力下降,治疗计划通常会受到更多限制。
AI框架使用医学图像个性化放疗剂量
该团队强调,PUO 方法提供了一种定量方法,可根据患者特定的临床因素和生物标志物,确定哪些患者可能受益于剂量递增或重新分配,同时还考虑了患者的几何形状和 OAR 剂量限制。
研究人员目前正在进行大规模回顾性研究,目标是开发一项采用 PUO 治疗计划策略的前瞻性临床试验。他们的研究围绕将患者数据和个性化结果预测直接整合到放射治疗计划中,目前重点关注肝癌、肺癌和头颈癌,在这些癌症中平衡放射治疗的积极和消极影响可能会显着影响患者的整体质量-生活。