
介绍根据最新的癌症统计,2020年全球估计新增癌症病例1,929万例,癌症死亡996万例。其中,中国新增癌症病例457万例,死亡300万例。手术、放疗和化疗是癌症治疗的标准方法。放疗是治疗原发性和转移性实体瘤、局部癌细胞扩散以及区域淋巴结转移最有效的方式之一。传统放疗(光子或电子)由于肿瘤位置、束流排列、技术和方式的限制,存在一定的缺点,会对肿瘤周围的重要器官和组织进行照射,从而导致某些短期和长期的并发症和后遗症。这些辐射并发症严重影响患者的生活质量。为了保证肿瘤周围正常器官和组织的辐射剂量不超过耐受剂量,必须减少对靶区的照射剂量,从而导致局部控制率降低。
最近几十年来,粒子放疗在美国、日本、德国等国家的临床实践中得到发展,包括质子和重离子(主要指碳离子)。根据粒子治疗合作组(PTCOG)公布的数据,截至2020年底,全球已有超过29万例患者接受了粒子治疗,其中包括近25万例质子和4万例碳离子。笔形束扫描质子治疗(PT)的共识指南,特别是用于胸部恶性肿瘤和前列腺癌的调强质子治疗,标志着质子治疗作为标准治疗的接受度越来越高。中国从1996年开始探索质子放疗,在过去的20多年里,多个质子项目被提上日程,但其中一些项目由于资金链断裂或维护成本过高而被停止。即便如此,中国目前有五家粒子放射治疗机构已经建成并正在接收患者,主要包括WPTC(淄博万杰)、SPHIC(上海)、HIMM(甘肃武威)、CGMH(台湾林口和高雄)及瑞金医院在2021年底建立的质子中心。中国是第四个使用碳离子治疗的国家。最近,基于最新研究数据的离子治疗指南(2020版)的制定,指导了中国离子治疗的临床实践,促进离子治疗的普及和应用。本次回顾将简要总结PT和碳离子放疗(CIRT)在中国的发展历史和现状,分析临床病例,并根据国情和离子放疗现状探讨质子和重离子设备在中国的发展和挑战。
质子和碳离子放射治疗的物理和放射生物学物理特性
质子和重离子医用加速器的优势主要体现在高能粒子束在人体组织中的线性能量传递(LET)的布拉格峰分布。由于人体组织中的这一特性,我们可以有选择地将能量主要沉积在肿瘤部位,而较少沉积在正常组织中,从而在不损害或较少损害正常组织的情况下消除癌症。在中国进行了一些光子、质子和碳离子放疗的治疗计划研究,这三种方式达到了相似的靶区适形。然而,在治疗局部复发性鼻咽癌(LR-NPC)时,PT和CIRT明显减少了危及器官(OARs)的剂量。
尽管碳离子和质子的物理特性非常相似,但与质子相比,碳离子放疗有如下特点:横向散射和射程偏移相对较小,束流晕较小;需要更高的能量才能到达深部肿瘤。因此,碳离子设备需要更大的加速器和束流递送系统。
放射生物学特征
RBE是指产生相同生物效应所需的两种辐射的吸收剂量比率。RBE受离子种类、剂量、LET、细胞和组织类型、生物终点和其他因素影响。在一定范围内,RBE随着LET的增加而增加。与光子或PT相比,CIRT具有更高的LET,根据被照射的组织和细胞可估计CIRT的RBE比光子RT大2~5倍。碳离子束的布拉格峰区出现在与RBE峰区相同的位置,这使得照射能量最大限度地作用于靶区,而正常组织受到照射的影响较小。碳离子利用其引起严重的簇状DNA双链断裂的生物特性来杀死肿瘤细胞(图1)。处于布拉格峰前端或尾部的大多数正常细胞可通过单链或双链断裂修复机制进行修复。电离辐射主要引起单碱基、单链断裂和双链断裂。质子和碳离子束对肿瘤细胞造成严重损伤,大部分细胞不能及时修复,导致细胞凋亡。前两类损伤主要由碱基切除修复途径修复。同源重组和非同源末端连接都参与DNA双链断裂的修复。一方面,放疗可以杀死双链断裂修复缺陷的细胞;另一方面,放疗产生的新抗原可以让肿瘤细胞被淋巴细胞处理而产生作用。同时,放疗可以促进细胞核和线粒体DNA分泌相关因子,如cGAS-STING介导的先天免疫增加免疫功能,共同促进肿瘤细胞的死亡。此外,也有报道说这些照射,特别是二次中子,可能诱发继发性肿瘤。
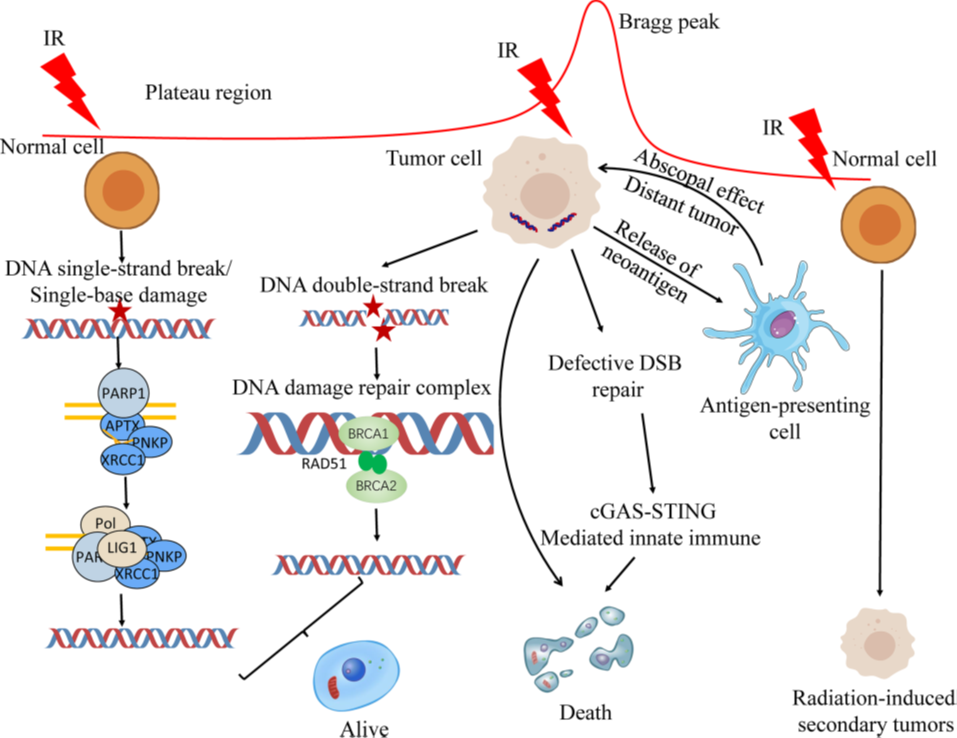
图1. 质子和碳离子放射治疗的生物学原理
除了高RBE外,碳离子还具有较低的氧增强率(OER)。OER指的是乏氧细胞和常氧细胞产生相同生物效应所需的剂量比例。由于肿瘤细胞生长快速,周围的坏死组织阻碍了氧气的供应,所以肿瘤细胞处于乏氧状态。与碳离子相比,光子、X射线和质子对乏氧的肿瘤细胞具有更高的OERs和更低的致死率。目前,中国有许多临床前放射生物学设施可以做体外和体内的研究(表1)。
表1.中国临床前放射生物学设施名单
