今天小编为大家分享的是2022年2月发表在European Journal of Nuclear Medicine and Molecular Imaging上的一篇文章,题目为“Fibroblast activation protein targeted therapy using [177Lu]FAPI-46 compared with [225Ac]FAPI-46 in a pancreatic cancer model”。文中,作者比较了β衰变核素177Lu和α衰变核素225Ac分别标记的FAPI-46在胰腺癌模型中的治疗效果。研究结果显示,[177Lu]FAPI-46和[225Ac]FAPI-46均可抑制肿瘤生长;二者相比,[177Lu]FAPI-46的治疗效果相对较慢,但持续时间较长。本文的通讯作者是大阪大学的Tadashi Watabe。

背景介绍
肿瘤基质占肿瘤质量的90%,在肿瘤的生长、转移和进展中发挥重要作用。成纤维细胞活化蛋白(fibroblast activation protein, FAP)在许多上皮癌间质的肿瘤相关成纤维细胞(cancer-associated fibroblasts, CAF)中高度表达,与不良预后相关。相反,FAP在正常组织中表达较低。因此,FAP是相关上皮癌诊断和治疗的良好靶点。在之前的研究中,68Ga、99mTc等核素标记的FAP抑制剂(FAPI)或FAPI衍生物,经PET/CT或SPECT/CT显像后可实现相关上皮癌的有效诊断。然而,关于FAPI治疗取得显著成功的报道还相对较少。作者在前期的研究中使用α衰变核素225Ac(t1/2=10 d)标记FAPI-04,并研究其对人胰腺癌的治疗效果。然而,FAPI通过肾脏快速排泄,且其生物半衰期与225Ac的物理半衰期不匹配。
在本研究中,作者尝试使用β衰变核素177Lu(t1/2=6.7 d)标记FAPI-46,比较[177Lu]FAPI-46和[225Ac]FAPI-46在胰腺癌模型中的治疗效果,以期找到半衰期较短的最佳放射性核素。
设计思路
作者制备了[18F]FAPI-74、[177Lu]FAPI-46和[225Ac]FAPI-46三种FAP靶向放射性药物。在PANC-1人胰腺癌异种移植小鼠模型中,使用[18F]FAPI-74进行PET/CT成像;研究[177Lu]FAPI-46和[225Ac]FAPI-46的生物分布;比较不同剂量的[177Lu]FAPI-46和[225Ac]FAPI-46对肿瘤的治疗效果,并评估潜在的副作用。
数据分析
首先,作者成功制备了[18F]FAPI-74、[177Lu]FAPI-46和[225Ac]FAPI-46三种放射性药物,三者的结构式如图1所示。

图1、[18F]FAPI-74、[177Lu]FAPI-46和[225Ac]FAPI-46的结构式
PANC-1异种移植小鼠经尾静脉注射[18F]FAPI-74后,分别进行动态和静态PET/CT扫描,并测量感兴趣区(肌肉、心脏、肺、肝、胆囊、肾、肠和肿瘤)的平均标准摄取值(SUVmean)和最大标准摄取值(SUVmax)。结果显示:[18F]FAPI-74被肾脏迅速清除,但肿瘤清除缓慢(图2. a);[18F]FAPI-74能较清晰地描绘肿瘤(图2. b);肿瘤内[18F]FAPI-74的积累显著高于大多数器官,但由于[18F]FAPI-74主要经胆汁和尿液排泄,胆囊和肾脏的摄取更高(图2. c)。然后,作者通过免疫组化证实了FAP在肿瘤基质中的高表达(图3)。

图2、(a)[18F]FAPI-74在PANC-1肿瘤和正常器官中的时间-放射性活度曲线。(b) PANC-1异种移植小鼠[18F]FAPI-74静态冠状PET成像(左)和PET/CT融合成像(右),箭头所指为肿瘤。(c)肿瘤和正常器官的SUVmean(上)和SUVmax(下)。

图3、(a)PANC-1异种移植物中FAP的免疫组化染色。(b)阴性对照。(放大倍数:400×)
经尾静脉向PANC-1异种移植小鼠注射[177Lu]FAPI-46和[225Ac]FAPI-46,探究二者在PANC-1异种移植小鼠中的生物分布。结果如图4所示,在给药后24 h [177Lu]FAPI-46在肿瘤、大肠和骨骼中积累相对较高,[225Ac]FAPI-46在肿瘤、脾、肝、胃中的积累相对较高。

图4、在给药后3 h和24 h,PANC-1异种移植小鼠中各器官[177Lu]FAPI-46(a)和 [225Ac]FAPI-46(b)的摄取百分比(%ID/g)。
随后,作者在PANC-1异种移植小鼠中比较两种放射性药物对肿瘤的治疗效果。经尾静脉将的[177Lu]FAPI-46或[225Ac]FAPI-46注射到PANC-1异种移植小鼠中,两组药物均设置有空白对照组。在观察期间,每周评估三次肿瘤大小和小鼠体重。所有动物在以下条件下进行安乐死: (1)当动物遭受不堪忍受的痛苦时;(2)当观察到活动显著减少或食物和水摄入量显著减少时;(3)当观察期结束时([177Lu]FAPI-46组44天,[225Ac]FAPI-46组32天)。
给予[177Lu]FAPI-46后,小鼠肿瘤大小和体重的变化如图5所示。通过多剂量组之间的比较,肿瘤的生长呈现抑制趋势。同时,与对照组相比,10 MBq组和30 MBq组小鼠的体重略有下降。给予[225Ac]FAPI-46后,10 kBq和30 kBq组小鼠肿瘤生长立即受到抑制,但3 kBq组的抑制作用非常轻微(图6. a)。3个剂量组中30 kBq组小鼠治疗效果最佳,但该组小鼠体重有一定下降(图6. b)。
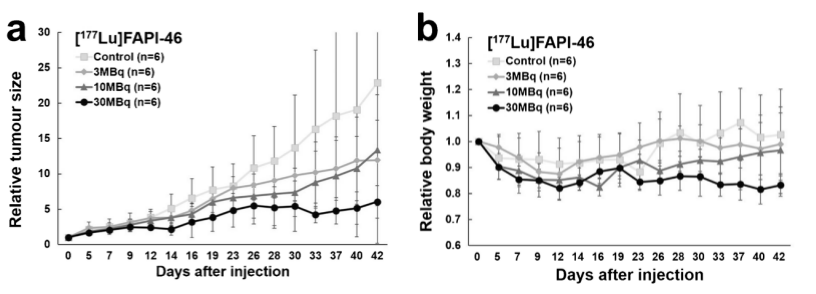
图5、[177Lu]FAPI-46组PANC-1异种移植小鼠相对肿瘤大小和相对体重的变化。
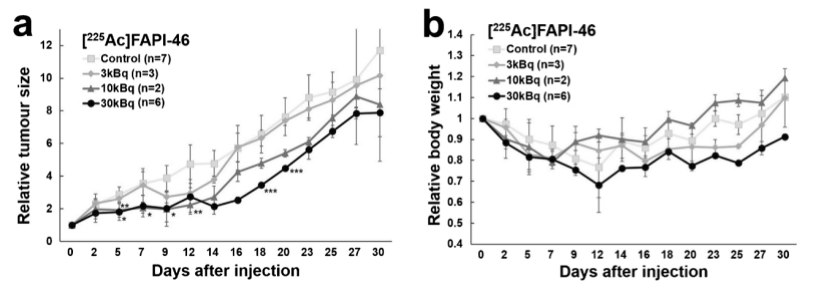
图6、[225Ac]FAPI-46组PANC-1异种移植小鼠相对肿瘤大小和相对体重的变化。
本研究中,[177Lu]FAPI-46的最小给药剂量(3 MBq/只)是根据临床实践中[177Lu]DOTA-TATE的推荐剂量基于小鼠体重换算后确定的,而[177Lu]FAPI-46设置的最大给药剂量(30 MBq/只)远超该值。同时,考虑到潜在的副作用,[225Ac]FAPI-46的最大给药剂量设定为每只小鼠30 kBq。观察期结束后,取各组小鼠的肿瘤和肾脏进行H&E染色。结果如图7所示,与对照组相比,各组小鼠肾脏没有观察到明显的组织学损害。

图7、H&E染色结果:[177Lu]FAPI-46组肿瘤(a)和肾脏(b);[225Ac]FAPI-46组肾脏(c)。(黄色标尺示50 μm)
总结与展望
这项研究揭示了[177Lu]FAPI-46和[225Ac]FAPI-46在PANC-1异种移植物中的治疗效果。研究的设计思路并不复杂,但存在一定的局限性,例如:只使用PANC-1一个细胞系进行评估;[225Ac]FAPI-46组的样本量不足;没有确定PANC-1模型中[177Lu]FAPI-46和[225Ac]FAPI-46的最大耐受剂量。
研究结果显示,[225Ac]FAPI-46对PANC-1异种移植物的治疗效果更快,但持续时间较短,而[177Lu]FAPI-46显示出缓慢、持久的治疗效果。这可能是因为两种放射性药物的靶细胞均是基质中的CAFs,而不是肿瘤细胞。由于基质和肿瘤细胞的不均匀分布导致不均匀的剂量分布,α粒子可能难以充分到达肿瘤细胞。肿瘤细胞更有可能受到[177Lu]FAPI-46的β粒子的照射,但其细胞杀伤性较α射线弱。
总体而言,[177Lu]FAPI-46和[225Ac]FAPI-46的治疗效果相当有限。与对照组相比,一些肿瘤抑制作用并不明显。一方面,FAPI在肿瘤中的滞留时间较短。虽已有研究者开发出相关的FAPI衍生物以提高肿瘤滞留率,但滞留率的显著提高并非易事,尚有待进一步的研究结果。另一方面,177Lu和225Ac较长的物理半衰期与FAPI的生物半衰期并不匹配。一些半衰期较短的放射性核素,如188Re(t1/2=17.0 h)或211At(t1/2=7.2 h),在给药早期即在肿瘤病灶内到达较高的放射性活度,有希望提高FAPI靶向治疗效果。在未来的研究中,可比较188Re和211At标记的FAPI的治疗效果,寻找最适合FAPI靶向治疗的放射性核素。