自世界卫生组织WHO定义了肿瘤疗效评估的方法,实体瘤疗效评价标准经历了好几代的发展与革新,从基于解剖结构影像的WHO标准(1979年)、RECIST标准(2000年)、RECIST 1.1标准(2009年),到基于分子代谢影像的EORTC标准(1999年)和PERCIST 1.0标准(2009年)[1-4]。
RECIST对WHO标准存在的问题进行了新的定义,如对需要进行评价的病灶作统一规定、明确规定所应测量的最小病灶的大小以及所应测量病灶的数量等。同时简化了测量步骤,提升了准确性。RECIST 1.1标准采用新的肿瘤大小测量方法,以肿瘤最长径的长度代替面积来代表肿瘤大小的一维测量方法(或称单径测量法),肿瘤大小测量的误差更小、重复性更好。它使用解剖影像(CT、MR)测量肿瘤大小的变化来判断疗效,但肿瘤疗效并不总与形态学相关,如淋巴瘤、恶性肉瘤、肝癌、间皮瘤及胃肠间质肿瘤,尽管治疗是有效的,但肿瘤的大小可能变化很小。
EORTC标准首次采用代谢显像评价肿瘤疗效,但存在局限性。它采用体重校正的SUV (即SUVbw) 作为疗效评价指标,其重复性差、变异大。PERCIST 1.0标准在EORTC基础上,推荐使用瘦体体重校正的SUV(即SUL),消除了脂肪对计算18F-FDG摄取的影响。采用SUL峰值 (SULpeak),即以肿瘤内最高摄取点为中心的、大小固定的球形VOI (VOIpeak)内SUL的最大可能平均值,替代传统的最大值或平均值作为评价指标。几乎不受噪声干扰,且与PET/CT系统或重建方法无关,受系统分辨率影响小。但在实际操作中,需注意VOIpeak可能超出肿瘤边界的情况。
RECIST 1.1标准与PERCIST 1.0标准在定义上存在相通性,也存在差异性。从下表中可以看出,他们都对可测量病灶、不可测量病灶、靶病灶、非靶病灶,以及靶病灶和非靶病灶的疗效评价进行定义。RECIST 1.1标准的诊断依据是测量病灶最长轴,观察解剖的改变,而PERCIST 1.0标准则是测量SUL峰值,观察代谢的变化。
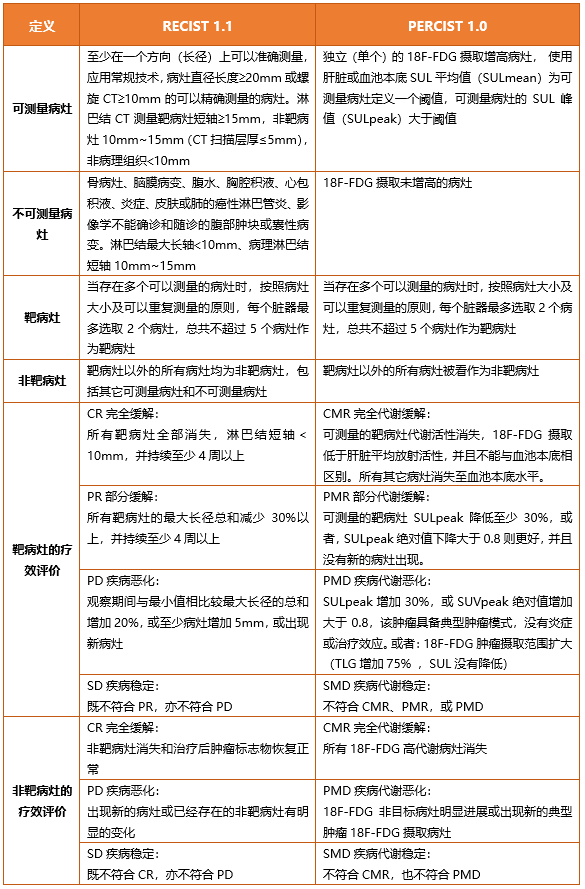
对于无FDG摄取的肿瘤病灶,可以选择RECIST 1.1标准,对于有FDG摄取的肿瘤病灶,PERCIST是首选。RECIST 1.1和 PERCIST标准在西门子分子影像图像后处理工作站上均已实现。其中,PET/CT成像更为常用的是PERCIST标准,配合使用西门子独家ALPHA人工智能引擎和MFS自动病灶勾画功能,可实现基于器官识别的智能解剖学配准,以及对全身高代谢区域的自动勾画、自动计算肿瘤代谢体积 (MTV) 、SUL(平均值、极值和峰值)和全身肿瘤负荷(TLG),方便临床医生完成精准的疗效评估及预后评价。