食管癌肿瘤位于纵膈或上腹部,邻近器官对放射线敏感的危及器官(OARs)有脊柱、肺和心脏。剂量递送的不确定性可能会破坏计划的剂量分布,因此有必要采取策略来确保靶区覆盖范围并避免整个治疗过程中OARs剂量过量。由于质子束的作用范围有限,质子剂量分布对密度变化更为敏感,治疗过程中的解剖学变化可能会对剂量分布产生潜在的严重影响。质子治疗(PT)剂量分布的潜在临床效益会受影响,导致局部控制下降或增加放射诱发不良事件。与光子治疗(XT)相比,PT可以显著降低OARs的剂量,而靶区剂量不受影响。
欧洲随机III期PROTECT试验比较了八个癌症中心质子与光子治疗食道癌的剂量分布和治疗计划的鲁棒性。所有中心使用4DCT扫描对4例接受28次50.4 Gy (RBE)的患者均分别进行一项优化PT和一项优化XT的计划。以超过99%靶区容积能接受到95%计划剂量(V95%iCTVtotal)评估治疗方法对摆位、射程和呼吸的鲁棒性。计划在第10分次时使用4DCT重新计算,所有患者均进行计划4DCT(pCT)和监测4DCT(sCT)扫描,并对呼吸运动和分次间解剖学变化的影响进行鲁棒性评估。
结果
所有PT和XT计划均符合V95%iCTVtotal>99%,所有PT和XT计划均符合呼吸和鲁棒性方案的V95%iCTVtotal>97%。图1显示了两例患者不同的剂量分布。在患者A中,平均心脏剂量(MHD)治疗最高,XT治疗时20~32 Gy;PT治疗时5~12 Gy。
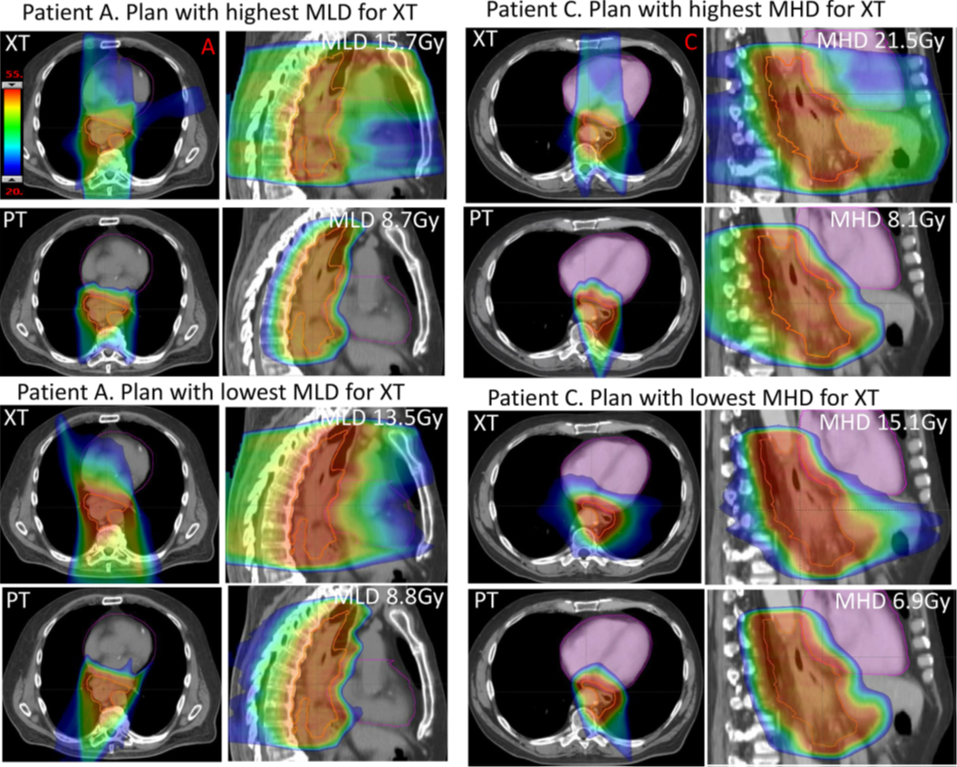
图1. 患者A和患者C的横断面和矢状图。20 Gy以上剂量用剂量洗色图表示(标尺见左上角)。iCTVtotal显示为红色。患者C的心脏显示为半透明紫色。
两种方式在肺部和心脏剂量差异很大,平均肺剂量(MLD)和MHD的差异分别为4.8 Gy[1.1;7.6](中位数[范围])和8.4 Gy[1.9;24.5](图2)。
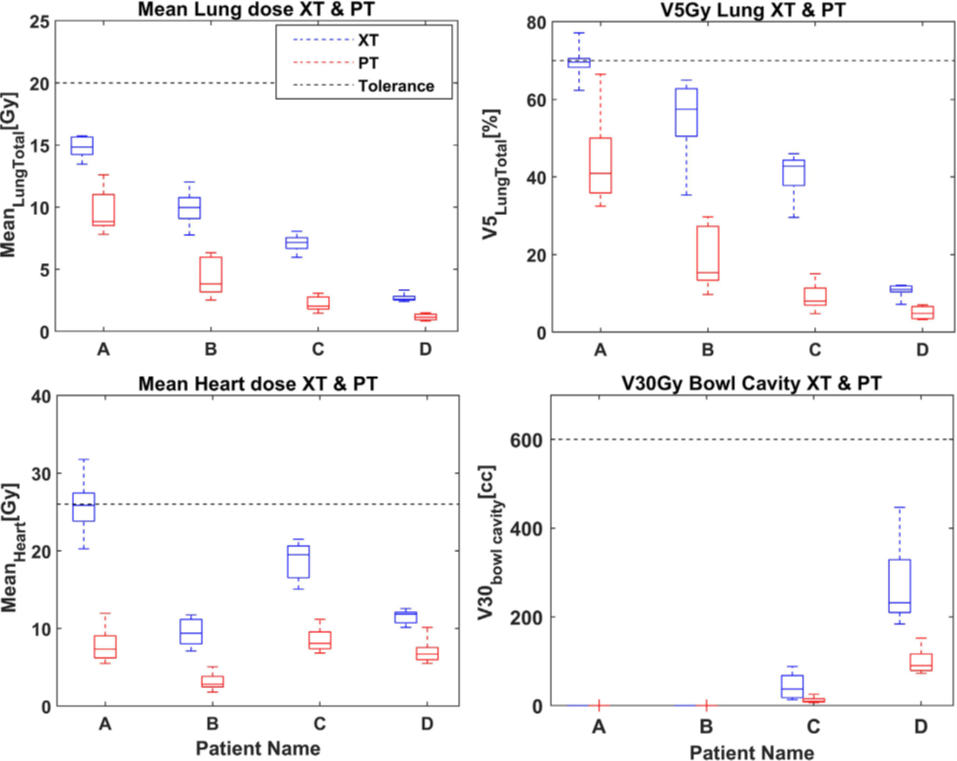
图2. 四位患者MLD、V5GyLung、MHD、v30Gy肠腔的箱线图。箱线图说明了中位数(水平线)、第1和第3个四分位范围。
4DCT显示出2位患者存在较大分次间解剖学变化,XT和PT在最坏情况鲁棒性情景中的最小V95%iCTVtotal分别为45% vs 57%和94% vs 72%。患者B的pCT和sCT中心鲁棒性评价如图3所示。4个PT中心,sCT的V95%iCTVtotal<97%,最小V95%iCTVtotal为94%(图3b)。5个XT中心,sCT的V95%iCTVtotal<97%,最小V95%iCTVtotal为45%。还有两例患者表现出轻微的分次间解剖学变化,最小V95%iCTVtotal大于85%。
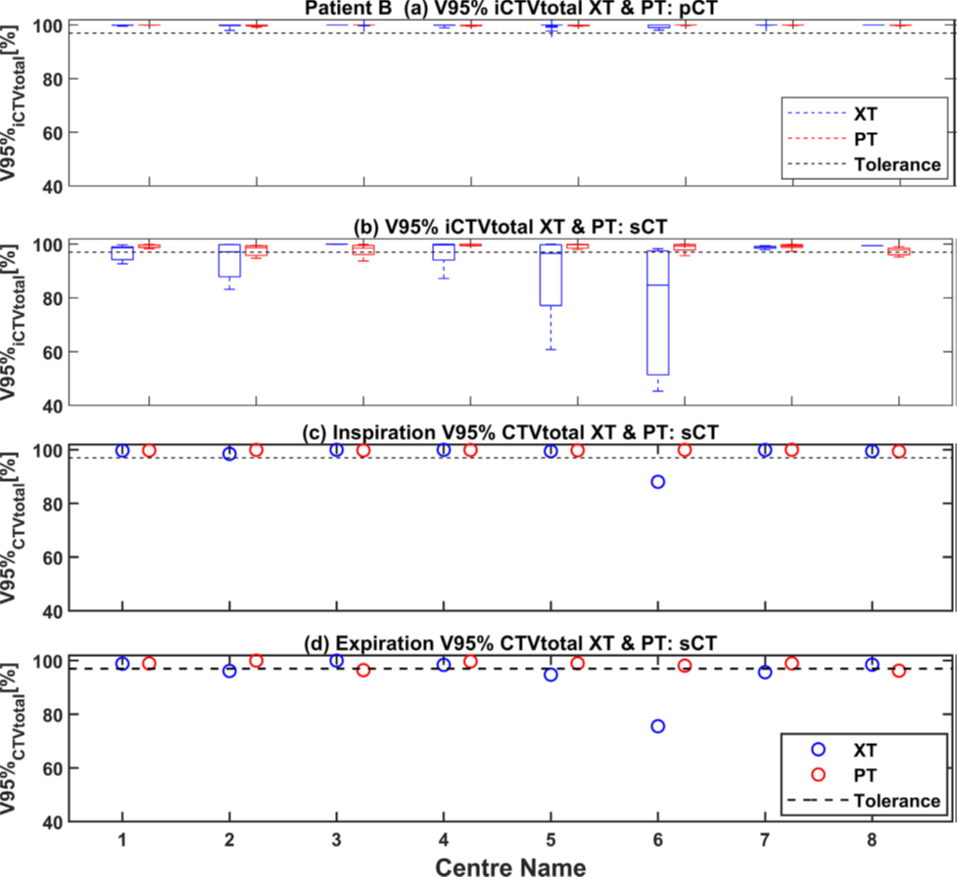
图3. 患者B的pCT和sCT中心鲁棒性评估。箱线图说明了中位数(水平线)、第1和第3四分位范围和最小/最大。XT计划用蓝色表示,PT计划用红色表示。虚线表示97%。面板a+b:箱线图显示八个中心pCT和sCT的iCTVtotal。注:中心8未对XT进行鲁棒性评估。
结论
PT和XT中肺部和心脏都有很大的剂量差。与XT比较,PT的分次间解剖学变化较小,靶区剂量较稳定。尽管所有中心的两种治疗方法都满足了治疗计划的第一优先限制(V95%iCTVtotal>99%),但OARs最大剂量以及计划鲁棒性都会因解剖学变化有很大改变。治疗过程中的解剖学改变会导致靶区剂量改变。XT因膈肌运动造成的影响比PT大。